决定元素种类的是
A.中子数 B.质子数 C.核外电子数 D.最外层电子数
B
【解析】
试题分析:质子数决定元素种类。选B。
考点:原子的结构。
点评:质子数决定元素种类,最外层电子数决定原子的化学性质。
归类整理是学习的一种重要方法。下列归类正确的是( )
A.氯、碘、汞都是非金属元素 B.醋酸,硝酸钾,二氧化硅都是化合物
C.铁、木头、玻璃都是热的良导体 D.太阳能,风能、核能是可再生能源
B
【解析】A、氯、碘都是非金属元素,汞是金属元素,错误;B、醋酸,硝酸钾,二氧化硅都是由不同种元素组成的化合物,正确;C、铁是热的良导体, 木头、玻璃不是热的良导体,错误;D、太阳能,风能是可再生能源,核能是不可再生能源,错误。故选B。
下列说法不正确的是( )
A.相同核电荷数的微粒不一定是同种元素 B.含氧的化合物不一定都是氧化物
C.由同种元素组成的物质一定是单质 D.原子核内不一定都有中子
C
【解析】
A、核电荷数相同的微粒可能是分子、原子、离子,不一定是同种元素,如水分子和氖原子的核电荷数相同,但不属于同种元素,正确;
B、氧化物是指由两种元素组成,其中一种元素是氧元素的化合物,含氧的化合物不一定只含有两种元素,比如硫酸含有氧元素,但不是氧化物,正确;
C、由同种元素组成的纯净物才叫单质,比如氧气和臭氧是由同种元素组成,但他们两个组成的是混合物,错误;
D、大部分原子核是由质子和中子构成,但不是所有的原子都有中子,比如氢原子就没有中子,错误。故选C。
【点睛】
化合物和单质都是纯净物中的一种,化合物是指由多种元素组成的纯净物,单质是指由一种元素组成的纯净物。
如图是五种粒子的结构示意图,下列说法正确的是
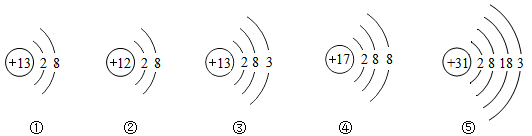
A.①②属于同种元素 B.③⑤化学性质相似
C.②③④均表示离子 D.②④形成的化合物是MgCl
B
【解析】
A、同种元素质子数相同,①②的质子数不相同,两者不属于同种元素,故A错误;B、元素的性质和最外层电子数的关系密切,最外层电子数相同则化学性质相似,由于③⑤的最外层电子数都是3,化学性质相似,故B正确;C、当质子数=核外电子数,为原子;当质子数≠核外电子数,为离子。③中质子数=核外电子数,为原子,②④中,质子数≠核外电子数,为离子,故C错误;D、②是镁离子,化合价为+2价,④是氯离子,化合价为-1价,②④形成的化合物是MgCl2,故D错误。故选B。
下列有关元素、原子、分子和离子的说法正确的是( )
A.决定元素化学性质的是原子的最外层电子数
B.原子可以构成分子,不能直接构成物质
C.分子是化学变化中的最小微粒
D.微粒得到或失去电子变成离子
A
【分析】
根据决定元素化学性质的因素;构成物质的粒子;分子的概念;微粒可能是分子、原子或离子,进行分析判断。
【详解】
A、决定元素化学性质的是原子的最外层电子数,选项说法正确;故符合题意;
B、原子可以构成分子,也能直接构成物质,选项说法错误;故不符合题意;
C、原子是化学变化中的最小微粒,选项说法错误;故不符合题意;
D、微粒可能是分子、原子或离子,微粒得到或失去电子,也可能是变为原子,选项说法错误;故不符合题意;
故选A
【点睛】
本题难度不大,掌握原子和离子的相互转化、决定元素化学性质的因素等是正确解答本题的关键。
本卷还有95题,登录并加入会员即可免费使用哦~

该作品由: 用户ysy分享上传
可圈可点是一个信息分享及获取的平台。不确保部分用户上传资料的来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系 可圈可点 ,我们核实后将及时进行处理。