下列说法正确的是( )
A.根据质量守恒定律,1 L氢气和1 L氧气反应生成2 L水
B.蜡烛完全燃烧后消失不见了,不遵循质量守恒定律
C.只有固体或液体间的反应才遵循质量守恒定律
D.铁丝在氧气中燃烧,生成四氧化三铁的质量等于参加反应的铁丝与氧气的质量之和
D
【详解】
A、质量守恒定律反映的是发生化学变化时物质间的质量关系不是体积关系,所以1L氢气和1L氧气反应生成2 L水不能由质量守恒定律得到,错误;
B、蜡烛属于化学变化,所以一定符合质量守恒定律,而完全燃烧后,蜡烛没有了,是因为生成了二氧化碳和水的扩散到空气中缘故,错误;
C、质量守恒定律施用于任何化学变化,而与反应物的状态无关,错误;
D、铁丝在氧气中燃烧生成四氧化三铁,由质量守恒定律,得到生成四氧化三铁的质量等于参加反应的铁丝与氧气的质量之和,正确。
故选D。
下列实验操作正确的是( )
A.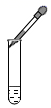 B.
B.
C.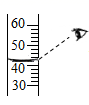 D.
D.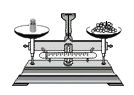
B
【详解】
A、使用胶头滴管滴加少量液体的操作,注意胶头滴管不能伸入到试管内或接触试管内壁,应垂直悬空在试管口上方滴加液体,防止污染胶头滴管,图中所示操作错误;
B、点燃酒精灯要用火柴点燃,不能用酒精灯引燃,图中所示操作正确;
C、量取液体时,视线与液体的凹液面最低处保持水平,图中视线没有与液体的凹液面最低处保持水平,图中所示操作错误;
D、托盘天平的使用要遵循“左物右码”的原则,应将将药品放在天平左盘中称量,图中所示操作错误。
故选B。
下列关于化学方程式“ ”的说法错误的是( )
”的说法错误的是( )
A.磷跟氧气在点燃的条件下反应生成五氧化二磷
B.每4个磷原子和5个氧分子在点燃的条件下反应生成2个五氧化二磷分子
C.参加反应的磷的质量的4倍加上参加反应的氧气的质量的5倍等于生成的五氧化二磷的质量的2倍
D.每31份质量的磷跟40份质量的氧气在点燃的条件下反应生成71份质量的五氧化二磷
C
【详解】
A、该反应可读作:磷跟氧气在点燃的条件下反应生成五氧化二磷,故选项说法正确。
B、微观上,该反应可读作:每4个磷原子和5个氧分子在点燃的条件下反应生成2个五氧化二磷分子,故选项说法正确。
C、参加反应的磷、氧气与生成的五氧化二磷的质量为(31×4):(32×5):(142×2)=31:40:71,故选项说法错误。
D、参加反应的磷、氧气与生成的五氧化二磷的质量为(31×4):(32×5):(142×2)=31:40:71,该反应可读作:每31份磷跟40份氧气在点燃的条件下反应生成71份五氧化二磷,故选项读法正确。
故选:C。
2.3 g某化合物在氧气中完全燃烧生成4.4 g二氧化碳和2.7 g水,则该化合物可能是( )
A.CH4 B.C2H4 C.C2H6 D.C2H5OH
D
【详解】
4.4g二氧化碳中碳元素的质量为:4.4g×![]() ×100%=1.2g,2.7g水中氢元素的质量为:2.7g×
×100%=1.2g,2.7g水中氢元素的质量为:2.7g×![]() ×100%=0.3g,根据质量守恒定律可得,2.3 g该化合物中碳元素的质量为:1.2g,氢元素的质量为:0.3g,氧元素的质量=23.g-1.2g-0.3g=0.8g,该化合物中碳元素、氢元素、氧元素的原子个数比为:
×100%=0.3g,根据质量守恒定律可得,2.3 g该化合物中碳元素的质量为:1.2g,氢元素的质量为:0.3g,氧元素的质量=23.g-1.2g-0.3g=0.8g,该化合物中碳元素、氢元素、氧元素的原子个数比为:![]() :
:![]() :
:![]() =2:6:1,故化合物的化学式为C2H6O。故选D。
=2:6:1,故化合物的化学式为C2H6O。故选D。
过氧化钠(Na2O2)可作呼吸面具中氧气的来源,它与二氧化碳反应后的生成物为( )
A.Na2CO3和H2 B.Na2O和O2 C.NaOH和O2 D.Na2CO3和O2
D
【解析】由题中信息及质量守恒定律可知,过氧化钠与二氧化碳反应生成氧气与另一种物质,另一种物质中必定含有钠元素和碳元素,故选D。
点睛:掌握化学反应前后元素的种类不变是解题关键。
本卷还有19题,登录并加入会员即可免费使用哦~

该作品由: 用户陈翀分享上传
可圈可点是一个信息分享及获取的平台。不确保部分用户上传资料的来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系 可圈可点 ,我们核实后将及时进行处理。