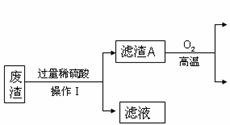
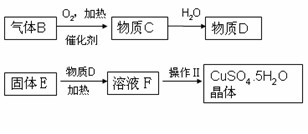
(2020·广饶期末)某炼铁废渣中含有大量CuS及少量的铁和铁的化合物(主要是氧化铁),工业上以该废渣为原料生产CuSO4•5H2O晶体的流程如图:
参考资料:CuS常温下和稀酸不发生反应。
(1)操作I的名称为________,该过程中玻璃棒的作用是________,由操作I得到的滤液中含有的溶质为________。写出滤渣A和氧气反应的化学方程式________。
(2)由固体E得到溶液F的过程通常需要加热,其作用是________,写出该步反应化学方程式:________。
(3)操作Ⅱ包括的步骤有加热浓缩、________、过滤。上述过程中可以循环利用的物质是________。
(1)过滤;引流;硫酸亚铁、硫酸铁、硫酸;2CuS+3O2 ![]() 2CuO+2SO2
2CuO+2SO2
(2)加快反应速率;CuO+H2SO4 ![]() CuSO4+H2O
CuSO4+H2O
(3)降温结晶;硫酸
【解析】(1)操作I的名称为过滤,该过程中玻璃棒的作用是引流,由操作I得到的滤液中含有的溶质为铁、氧化铁分别和硫酸反应生成的硫酸亚铁、硫酸铁,还有过量的硫酸;滤渣A是硫化铜,和氧气在高温条件下反应生成氧化铜和二氧化硫,反应的化学方程式:2CuS+3O2 ![]() 2CuO+2SO2;(2)由固体E得到溶液F的过程通常需要加热,其作用是加快反应速率;该步反应化学方程式 CuO+H2SO4
2CuO+2SO2;(2)由固体E得到溶液F的过程通常需要加热,其作用是加快反应速率;该步反应化学方程式 CuO+H2SO4 ![]() CuSO4+H2O;(3)操作Ⅱ包括的步骤有加热浓缩、降温结晶、过滤,上述过程中可以循环利用的物质是D(硫酸)。
CuSO4+H2O;(3)操作Ⅱ包括的步骤有加热浓缩、降温结晶、过滤,上述过程中可以循环利用的物质是D(硫酸)。
【分析】解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论。
(2020·乐平模拟)表实验方案中,能达到实验目的是________
| 选项 | 实验目的 | 实验方案 |
| A | 分离铜粉和铁粉 | 加入过量的稀盐酸,过滤 |
| B | 除去氯化钠固体中的少量碳酸钠 | 加入适量稀盐酸,充分反应后,蒸发 |
| C | 检验二氧化碳气体中含有少量一氧化碳 | 将混合气体依次通过灼热的氧化铁和澄清石灰水,观察澄清石灰水的变化 |
| D | 鉴别固体氢氧化钠和固体氯化铵 | ________ |
B;加水,观察温度变化
【解析】A、加入过量的稀盐酸,铁能与稀盐酸反应生成氯化亚铁和氢气,铜不与稀盐酸反应,过滤,得到铜粉,但是得不到铁粉,达不到分离的目的,不符合题意;
B、加入适量稀盐酸,碳酸钠能与稀盐酸反应生成氯化钠、二氧化碳和水,充分反应后,蒸发,可得氯化钠固体,符合题意;
C、将混合气体依次通过灼热的氧化铁和澄清石灰水,一氧化碳能与氧化铁在高温的条件下反应生成铁和二氧化碳,二氧化碳能使澄清石灰水变浑浊,但是原有的二氧化碳也能使澄清石灰水变浑浊,无法检验二氧化碳气体中含有少量一氧化碳,不符合题意;
D、氢氧化钠溶于水放出大量的热,使温度升高,氯化铵溶于水吸热,使温度降低,故可加水,观察温度变化。
故答案为:B,填:加水,观察温度变化。
【分析】A、根据金属活动性顺序中排列在氢之前的金属和酸能反应分析
B、根据碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳分析
C、根据一氧化碳具有还原性分析
D、根据氢氧化钠溶解放热分析
(2020·南昌模拟)下列实验操作中能达到实验目的的是(________)
| 选项 | 物质 | 目的 | 主要实验操作 |
| A | CaO固体中混有CaCO3 | 除杂 | 加水溶解并过滤 |
| B | NaCl溶液中含有HCl | 检验 | 取样,滴加无色酚酞溶液,观察 |
| C | KNO3固体混有少量NaCl | 提纯 | 溶解,蒸发浓缩,降温结晶,过滤,洗涤烘干 |
| D | 羊毛、棉线 | 鉴别 | ________ |
C;取样灼烧
【解析】A、氧化钙和水反应生成氢氧化钙,该过程中将原物质除去,不符合除杂的原则。A不符合题意;
B、氯化钠的水溶液呈中性,稀盐酸的水溶液呈酸性。中性或酸性的溶液都不能使无色酚酞溶液变红,所以无明显现象。B不符合题意;
C、硝酸钾固体中混有少量的氯化钠,为了提纯硝酸钾,由于硝酸甲的溶解度随温度的升高而增大而且变化趋势明显,氯化钠虽然溶解度也随温度的升高而增大,但是变化趋势不明显。所以根据此,可以将混合物配制成溶液后,蒸发浓缩,随后将溶液降温,从而析出硝酸钾晶体。将硝酸钾晶体和溶液过滤后,将硝酸钾晶体洗涤烘干,得到提纯后的硝酸钾固体。C符合题意;
D、羊毛中含有蛋白质,灼烧会有烧焦羽毛的气味,而棉线不会。所以可以灼烧闻气味来鉴别。
故答案为:C、取样灼烧闻气味。
【分析】物质除杂时坚持两个原则,其一是除杂剂主要成分不反应,其二是除杂剂和杂质反应时不能产生新的杂质,据此分析
(2020·乐平模拟)有4瓶常用溶液:①BaCl2溶液,②NaCl溶液,③Na2SO4溶液,④CuSO4溶液。不用其他试剂,可通过实验方法将它们一一鉴别开来,鉴别出来的先后顺序可能是( )
A. ①④③② ![]() B. ①③④②
B. ①③④② ![]() C. ④①③②
C. ④①③② ![]() D. ④①②③
D. ④①②③
C
【解析】溶液颜色为蓝色的是硫酸铜,能与硫酸铜反应生成白色沉淀的是氯化钡,能与氯化钡反应生成白色沉淀的是硫酸钠,剩下的是氯化钠,故鉴别出来的先后顺序可能是:④①③②。
故答案为:C。
【分析】根据复分解反应的条件进行分析
(2020·德州模拟)下列物质存放在烧杯中一段时间后,质量变大且没有发生化学变化的是( )
A. 氢氧化钠 ![]() B. 浓硫酸
B. 浓硫酸 ![]() C. 浓盐酸
C. 浓盐酸 ![]() D. 生石灰
D. 生石灰
B
【解析】A. 氢氧化钠会与空气中的二氧化碳反应生成碳酸钠和水,质量变大,但是发生了化学变化,故不符合题意;
B. 浓硫酸具有吸水性,会吸收空气中的水蒸气,质量变大,没有发生化学变化,故符合题意;
C. 浓盐酸具有挥发性,会挥发出氯化氢气体,质量变小,故不符合题意;
D. 生石灰能与水反应生成氢氧化钙,质量变大,但是发生了化学变化,故不符合题意。
故答案为:B。
【分析】变化时没有生成其它物质的变化,叫物理变化。
变化时都生成新物质的变化,叫做化学变化。
本卷还有45题,登录并加入会员即可免费使用哦~

该作品由: 用户丛玮分享上传
可圈可点是一个信息分享及获取的平台。不确保部分用户上传资料的来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系 可圈可点 ,我们核实后将及时进行处理。