如图7-4-1是粗盐提纯过程中的几项实验操作,请回答下列问题。
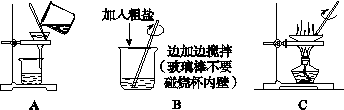
图7-4-1
(1)除去粗盐中难溶性杂质的操作步骤的顺序为__________。
(2)操作A中玻璃棒的作用是______________,操作B中玻璃棒的作用是______________,操作C中玻璃棒的作用是________________________________________________________。
(3)下列各组试剂也可利用上述操作进行分离的是________。
A. 从碳酸钠和碳酸钙的固体混合物中分离出碳酸钙
B.从KCl和MnO2的混合物中分离出KCl
C. 从硝酸钾和氯化钠的混合物中分离出硝酸钾
D. 除去混在铜粉中的铁粉
(1)BAC (2)引流 搅拌,加速粗盐的溶解
搅拌,防止液体因局部温度过高而造成液滴飞溅 (3)B
从“降温结晶”“蒸发结晶”或“过滤”中为下列混合物分离或除去杂质选择一种主要的方法。
(1)从硝酸钾的饱和溶液中提取硝酸钾晶体__________________________。
(2)从海水中得到食盐采用的方法是________________________。
(3)要除去粗盐中的泥沙,可采用的方法是____________________。
(4)要除去硝酸钾中混有的少量氯化钠,可采用的方法是________________。
(1)降温结晶 (2)蒸发结晶 (3)过滤 (4)降温结晶
小明同学在做“粗盐中难溶性杂质的去除”实验时,用到了如图7-4-6所示的装置。
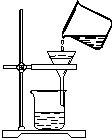
图7-4-6
(1)请指出该装置图中的一处错误:______________________________。
(2)改正装置后过滤,发现滤液仍然浑浊,其原因可能是什么?________________________________________________________________________(写出一条即可)。
(3)经初步提纯所得精盐是否为纯净物?请写出你的判断和理由:__________________
________________________________________________________________________________________________________________________________。
(1)没有用玻璃棒引流
(2)滤纸破损(或液面高于滤纸边缘或接滤液的烧杯不干净,合理即可)
(3)不是纯净物,因为经初步提纯所得精盐中仍含有可溶性杂质
苯甲酸有抑制真菌、细菌、霉菌生长的作用,常用作药物或防腐剂。苯甲酸常温下为片状或针状结晶,在100 ℃时会迅速升华,苯甲酸在水中的溶解度见下表:
| 温度 | 20 ℃ | 25 ℃ | 50 ℃ | 75 ℃ | 95 ℃ |
| 溶解度 | 0.17 g | 0.35 g | 0.95 g | 2.2 g | 6.8 g |
为了提纯某苯甲酸样品(其中含有难溶于水的杂质),某化学小组进行了如下实验:
(1)取约1 g样品放入烧杯中,加入50 mL蒸馏水充分搅拌,发现样品几乎没溶解。原因是苯甲酸属于________(填“易溶”“可溶”“微溶”或“难溶”)物。
(2)将烧杯放在石棉网上加热至样品充分溶解,再加少量蒸馏水,然后趁热过滤。趁热过滤的目的是_________________________________________________________。
(3)将所得滤液____________,使苯甲酸以晶体的形式析出,然后过滤得到较纯净的苯甲酸晶体。
(4)(3)中过滤后的滤液是苯甲酸的_________(填“饱和”或“不饱和”)溶液。
(1)微溶 (2)避免过滤除去难溶性杂质时,苯甲酸因降温析出而损耗
(3)降温结晶 (4)饱和
下列关于结晶的说法不正确的是( )
A. 结晶是指有规则几何形状的晶体从溶液中析出的过程
B.不同晶体从溶液中析出后,其几何形状可能不相同
C.结晶必须在蒸发溶剂的时候才能进行
D.把硝酸钾晶体从其溶液中结晶出来最好采用冷却结晶法
C
本卷还有7题,登录并加入会员即可免费使用哦~

该作品由: 用户enh分享上传
可圈可点是一个信息分享及获取的平台。不确保部分用户上传资料的来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系 可圈可点 ,我们核实后将及时进行处理。