某同学在探究“酸与碱能否发生反应”时,用稀氢氧化钠溶液、稀盐酸和酸碱指示剂进行实验的过程如图6-Z-1所示。图中所加试剂①②③分别是( )

图6-Z-1
A. 稀氢氧化钠溶液、石蕊溶液、稀盐酸
B.稀盐酸、石蕊溶液、稀氢氧化钠溶液
C.稀氢氧化钠溶液、酚酞溶液、稀盐酸
D.稀盐酸、酚酞溶液、稀氢氧化钠溶液
C
实验小组在探究“酸与碱能否发生反应”时,进行了如图6-Z-2所示实验。请根据实验回答:
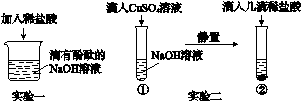
图6-Z-2
探究实验一: 酸能否与可溶性碱发生化学反应。
甲同学进行了实验一,能观察到的明显现象是________________________,同时测定反应后溶液的pH=2,说明酸能与可溶性碱发生化学反应。
探究实验二: 酸能否与难溶性碱发生化学反应。
乙同学进行了实验二,当滴入几滴稀盐酸后,发现试管②中无明显变化,于是得出“酸不能与难溶性碱反应”的结论。
丙同学对此产生怀疑,并利用实验后的物质继续探究:
[分析] 丙同学测定试管②中上层清液的酸碱度,读出pH=12,说明上层清液中的溶质是____________________________。
[解释] 丙同学由此认为乙同学的结论不正确,原因是________________________。
[验证] 丙同学利用上述实验后的废液进行实验,将试管②中物质全部倒入一大烧杯中,静置,再将实验探究一所得溶液缓慢逐滴加入,说明酸能与难溶性碱发生化学反应的现象是________________________________________________________________________。
探究实验一:溶液由红色变为无色
探究实验二:[分析] Na2SO4、NaCl、NaOH
[解释] 几滴盐酸先与氢氧化钠反应,不能确定酸不与难溶性碱反应(合理即可)
[验证] 蓝色沉淀逐渐溶解(或蓝色沉淀部分溶解或溶液变为蓝色)
某化学课堂围绕“酸碱中和反应”,将学生分成若干小组开展探究活动。请你和他们一起完成以下实验探究。
[演示实验] 将一定量稀盐酸加入到盛氢氧化钙溶液的小烧杯中,该反应的化学方程式是__________________________________。
[查阅资料] CaCl2溶液显中性。
[提出问题] 实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质的成分是什么?
[猜想与假设] 针对疑问,甲组同学猜想如下。
猜想Ⅰ:只有CaCl2;
猜想Ⅱ:有________________;
猜想Ⅲ:有CaCl2和Ca(OH)2;
猜想Ⅳ:有CaCl2、HCl和Ca(OH)2。
乙组同学对以上猜想提出质疑,认为猜想Ⅳ不合理,其理由是________________________________________________________________________。
[实验探究] 为了验证其余猜想,各小组进行了下列三个方案的探究。
| 实验方案 | 滴加紫色石蕊溶液 | 通入CO2 | 滴加Na2CO3溶液 |
| 实 验 操 作 |
|
|
|
| 实验现象 | ________________ | ________________ | 产生白色沉淀 |
| 实验结论 | 溶液中含有Ca(OH)2 | 溶液中含有Ca(OH)2 | 溶液中含有Ca(OH)2 |
[得出结论] 通过探究,大家确定猜想Ⅲ是正确的。
[评价反思] (1)丙组同学认为加Na2CO3溶液产生白色沉淀,不能证明溶液中一定含有Ca(OH)2,请你帮助他们说明原因:_________________________________________________。
(2)在分析反应后所得溶液中溶质的成分时,除了要考虑生成物外,还需要考虑_______________________________________________________________________________。
演示实验] 2HCl+Ca(OH)2===CaCl2+2H2O
[猜想与假设] CaCl2和HCl HCl和Ca(OH)2不能共存
[实验探究] 石蕊溶液变蓝 溶液变浑浊
[评价反思] (1)CaCl2与Na2CO3反应也会生成白色沉淀
(2)反应物是否过量
室温下,将稀盐酸慢慢滴入装有氢氧化钠溶液的烧杯中,利用温度计测出烧杯中溶液的温度。溶液温度随加入盐酸的质量而变化的曲线如图6-Z-3所示:
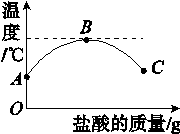
图6-Z-3
(1)由图可知,盐酸与氢氧化钠溶液发生的中和反应是________(填“吸热”“放热”或“无热量变化”)反应。
(2)在A处溶液中加入石蕊溶液,溶液呈________色。
(3)B处溶液的溶质是____________(填化学式)。
(4)从B到C的过程中,溶液的pH逐渐________(填“增大”“减小”或“无变化”)。
(5)在C点溶液中加入碳酸钙,现象为________________________,反应的化学方程式为__________________________________________。
(1)放热 (2)蓝 (3)NaCl (4)减小
(5)有气泡产生 CaCO3+2HCl===CaCl2+H2O+CO2↑
小青按如图6-Z-5所示操作进行酸碱中和反应的实验,回答问题。

图6-Z-5
(1)图E是稀释浓硫酸的操作示意图,甲烧杯中的物质应是____________。
(2)小青观察到图C中溶液由红色变为无色,认为氢氧化钠与硫酸恰好完全反应,化学方程式是______________________________________。
(3)小楚想用紫色石蕊溶液、氧化铜粉末、碳酸钠溶液、氯化钡溶液进一步确定反应后的无色溶液中溶质的成分,其中不能达到目的的是________________。
(1)浓硫酸
(2)H2SO4+2NaOH===Na2SO4+2H2O
(3)氯化钡溶液

该作品由: 用户王提分享上传
可圈可点是一个信息分享及获取的平台。不确保部分用户上传资料的来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系 可圈可点 ,我们核实后将及时进行处理。