科学探究小组在探究酸的性质时,做了如下实验:向放有少量CuO粉末的试管中加入6毫升盐酸,观察到黑色粉末很快溶解,并得到蓝绿色溶液。而向放有少量CuO粉末的试管中加入6毫升硫酸溶液,常温下无明显现象。为什么会产生这种差异呢?
[建立猜想] ①两种酸溶液的pH不同(注:pH相同,则单位体积溶液中H+数目相同)。
②两种酸溶液中的________不同。
[实验过程]
| 实验 次数 | 试剂 | 实验 条件 | 实验现象 |
| 1 | 0.2克CuO粉末+6毫升pH=0的盐酸 | 常温 | 黑色粉末很快溶解,溶液呈蓝绿色 |
| 2 | 0.2克CuO粉末+6毫升pH=0的硫酸 | 常温 | 无明显现象 |
| 3 | 0.2克CuO粉末+6毫升pH=0的硫酸+0.35克NaCl | 常温 | 黑色粉末很快溶解,溶液呈蓝绿色 |
| 4 | 0.2克CuO粉末+6毫升pH=0的硫酸+0.35克________ | 常温 | 无明显现象 |
[实验结论] 常温下,pH相同的盐酸和硫酸溶液与CuO反应现象出现差异的原因是由于________促进了反应的进行。
[建立猜想] 酸根离子(或阴离子)
[实验过程] Na2SO4
[实验结论] Cl-
[解析] [建立猜想] 当两种酸溶液的pH相同时,仍然出现上述实验中现象的差异,可能原因就是盐酸和硫酸溶液中的酸根离子(或阴离子)不同导致。[实验过程] 为了验证上述猜想②,设计实验3、4进行对比,在其他条件相同的情况下,实验3加入了NaCl,则实验4应加入等质量的Na2SO4进行对比,由此可获得正确的结论。[实验结论] 由上述3、4两个对比实验的现象可以获得的结论:常温下,pH相同的盐酸和硫酸溶液与CuO反应现象出现差异的原因是由于氯离子(Cl-)促进了反应的进行。
某同学查阅资料得知,实验室常用电石(主要成分是CaC2)与水反应制取乙炔(C2H2),反应的化学方程式为CaC2+2H2O===Ca(OH)2+C2H2↑(电石中的杂质不溶于水且不与水反应,也不与Na2CO3溶液反应)。在实验室中,该同学把一定量的CaC2加入Na2CO3溶液中充分反应后过滤,得到滤渣和滤液,并对滤液的成分进行探究。
[提出问题] 滤液中溶质的成分是什么?
[猜想与假设] 猜想一:NaOH、Na2CO3;猜想二:NaOH;猜想三:NaOH、Ca(OH)2。
[分析与推理] 分析一:若猜想一成立,说明实验中加入的CaC2量少,CaC2与水反应生成的Ca(OH)2与Na2CO3反应后,Na2CO3剩余。
分析二:若猜想二成立,说明实验中加入的CaC2与水反应生成的Ca(OH)2与Na2CO3恰好完全反应。
分析三:若猜想三成立,说明实验中加入的CaC2量多,CaC2与水反应生成的Ca(OH)2与Na2CO3反应后,Ca(OH)2剩余。
由以上分析可推知:反应后滤液中一定存在的溶质是________(填化学式,下同),可能存在的溶质是________和________。对可能存在的溶质需要进一步实验验证。
[实验验证]
| 实验序号 | 实验操作 | 实验现象 | 实验结论 |
| 实验一 | 取少量滤液于试管中,向其中加入过量稀盐酸 | 无气泡产生 | 猜想________不成立 |
| 实验二 | 取少量滤液于试管中,向其中滴加适量碳酸钠溶液 | ________________________________________________________________________ ________________________________________________________________________ | 猜想三成立,发生反应的化学方程式为____________ |
[拓展延伸] 若向CuCl2溶液中加入少量CaC2,充分反应,可观察到有气泡产生,同时出现蓝色的________(填化学式)沉淀。实验室保存电石应注意________。
[分析与推理] NaOH Ca(OH)2 Na2CO3
[实验验证] 一 有白色沉淀生成
Ca(OH)2+Na2CO3===CaCO3↓+2NaOH
[拓展延伸] Cu(OH)2 密封保存
某兴趣小组用图KZ9-1中Ⅰ装置进行实验时发现,烧杯中饱和石灰水先变浑浊,后逐渐澄清。


图KZ9-1
(1)写出甲装置中发生反应的化学方程式:________________________;石灰水变浑浊是因为生成了________(填化学式)。
(2)为探究“饱和石灰水浑浊后变澄清的原因”,该小组同学开展了如下活动:
[查阅文献] 碳酸钙(碳酸钠等)与二氧化碳、水反应生成可溶于水的碳酸氢钙(碳酸氢钠等)。
[提出假设] 假设 1:挥发出的HCl使浑浊变澄清;
假设 2:________________________________________________________________________。
[设计实验] 为除去 CO2中的HCl,小华在图Ⅰ中甲、乙装置之间增加图Ⅱ装置, 装置的连接顺序是甲→________→________(填管口序号)→乙;其中存放的试剂合理是________(填序号)。
A.浓硫酸 B.饱和Na2CO3溶液
C.NaOH 溶液 D.饱和NaHCO3溶液
[实验现象] 饱和石灰水浑浊后,继续通入足量CO2,沉淀部分溶解但最终并未完全澄清。
[得出结论] 由以上探究可得出结论是________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
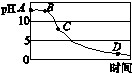
图KZ9-2
(3)该兴趣小组在老师指导下,用pH传感器测得图Ⅰ烧杯中溶液的pH随通入时间的变化曲线如图KZ9-2所示。
①AB段pH不变的可能原因是________________________________________________________________________
____________;D点所得溶液的成分除 H2O外还有______________。
②BC段发生的化学方程式主要有________________________________________________________________________
________________________________________________________________________。
(1)2HCl+CaCO3===CaCl2+CO2↑+H2O
CaCO3
(2)[提出假设] 产生的CO2使浑浊变澄清
[设计实验] b a D
[得出结论] 挥发出的HCl使饱和石灰水产生的浑浊最终变澄清;CO2只能使饱和石灰水产生的沉淀部分溶解,不能最终使其变澄清
(3)①一开始排出来的是空气,不会使溶液pH明显变化 CaCl2和HCl(或Ca2+、H+、Cl-)
②Ca(OH)2+CO2===CaCO3↓+H2O、2HCl+Ca(OH)2===CaCl2+2H2O
(1)如图KZ9-3是实验室制取气体的一些装置,据图回答:
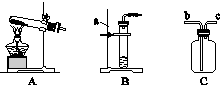
图KZ9-3
①图B中仪器a的名称是________。
②用高锰酸钾制取氧气的发生装置是________(填序号),若用C装置收集氧气,验满时,应将带火星的木条放在________(填“b”或“c”)端导管口,若木条复燃,说明氧气已满。
(2)小明在帮老师整理实验室时,发现一瓶未密封的KOH固体,对其成分提出以下假设,并在老师的指导下进行实验探究。
[查阅资料] ①KOH与NaOH的化学性质相似。请用化学方程式解释KOH变质的原因是________________________________。
②K2CO3溶液呈碱性,BaCl2溶液、KCl溶液呈中性。
[猜想假设] 假设Ⅰ:只含KOH;假设Ⅱ:含KOH和K2CO3;假设Ⅲ:只含K2CO3。
[进行实验]
| 实验操作步骤 | 实验现象 | 实验结论 |
| ①取少量样品于试管中,加入足量的稀盐酸 | 有气泡 产生 | 假设____ 不正确 |
| ②另取少量样品于试管中,加水溶解,加入过量的BaCl2溶液,振荡,静置 | ________________________________________________________________________ | |
| 假设Ⅲ 正确 |
③取②中上层清液,滴加无色酚酞溶液,________________________________________________________________________[问题讨论] 步骤②中加入过量BaCl2溶液的作用是________________________________________________________________________。
[拓展应用] 完全变质的KOH也有利用价值,从K2CO3的组成或性质看,这瓶变质的试剂在农业上的用途是________________________________________________________________________。
(1)①铁架台 ②A c
(2)[查阅资料] 2KOH+CO2===K2CO3+H2O
[进行实验] Ⅰ 产生白色沉淀 酚酞不变色
[问题讨论] 使K2CO3完全反应完,排除对KOH检验的干扰
[拓展应用] 作钾肥
碳酸氢钠是小苏打的主要成分,在生产和生活中有许多重要的用途。化学课上,同学们为了解碳酸氢钠的性质,将一定质量的碳酸氢钠和稀硫酸混合,充分反应后,有气泡逸出,写出该反应的化学方程式:____________________________________________。同学们对反应后溶液中溶质的成分进行了探究:认为除一定含有硫酸钠外可能还含有其他成分,因此进行了猜想并做了如下实验。
[实验用品] pH试纸、锌片、氧化铜粉末、稀硫酸、氢氧化钠溶液、氯化钡溶液。
[猜想与假设] 反应后溶液中溶质的组成成分可能有哪些?
猜想一:硫酸钠;猜想二:硫酸钠、碳酸氢钠;猜想三:硫酸钠、硫酸。
[实验探究] 同学们取反应后的溶液用不同方案进行如下实验,请根据结论完成下表。
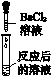
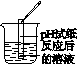
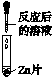
| 实验 方案 | A | B | C | D |
| 实验 操作 |
|
|
|
|
| 实验 现象 | ________ | 产生白色沉淀 | 试纸变色, 对照标准 比色卡,pH ________7 | ________ ________ |
| 实验 结论 | 猜想二 不正确 | 猜想三 正确 | 猜想三正确 | 猜想三 正确 |
[得出结论] 猜想三正确。
[评价反思] (1)老师对同学们能用多种方案进行探究,并且得出正确的实验结论给予肯定,同时指出探究中存在一处明显错误操作的是方案________。
(2)有同学对实验方案B的结论提出了质疑,认为仅凭此现象不能得出猜想三正确,请说明理由:________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
[总结提高] 依据所给实验用品,请你设计不同的方案确认猜想三是正确的:________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
NaHCO3+H2SO4===Na2SO4+2CO2↑+2H2O
[实验探究] 无现象 <
有气泡产生,锌片逐渐溶解
[评价反思] (1)C
(2)因为溶液中的硫酸钠与氯化钡溶液反应也生成硫酸钡白色沉淀,此现象的产生,不能证明溶液中含有硫酸
[总结提高] 取少量的氧化铜粉末于试管中,向试管中加入反应后的溶液,观察到试管中的黑色粉末溶解,溶液变为蓝色,则猜想三正确

该作品由: 用户蔡佳莹分享上传
可圈可点是一个信息分享及获取的平台。不确保部分用户上传资料的来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系 可圈可点 ,我们核实后将及时进行处理。