下列变化,一定是化学变化的是( )
A.铁水铸成锅 B.瓷器破碎 C.酒精溶解碘 D.铁矿石炼成铁
【考点】化学变化和物理变化的判别.
【专题】物质的变化与性质.
【分析】化学变化是指有新物质生成的变化,物理变化是指没有新物质生成的变化,化学变化和物理变化的本质区别是否有新物质生成;据此分析判断.
【解答】解:A、铁水铸成锅过程中没有新物质生成,属于物理变化.
B、瓷器破碎过程中只是形状发生改变,没有新物质生成,属于物理变化.
C、酒精溶解碘过程中没有新物质生成,属于物理变化.
D、铁矿石炼成铁过程中有新物质铁生成,属于化学变化.
故选D.
【点评】本题难度不大,解答时要分析变化过程中是否有新物质生成,若没有新物质生成属于物理变化,若有新物质生成属于化学变化.
化学与我们生活密切相关,下列有关说法不正确的是( )
A.铁制品表面生锈后,形成保护膜,会减慢锈蚀速度
B.洗涤剂能洗掉油污是因为洗涤剂具有乳化功能
C.菜刀用后立即用抹布擦干防止生锈
D.铝制锅盖不可以用钢刷擦洗
【考点】金属锈蚀的条件及其防护;乳化现象与乳化作用;金属的化学性质.
【专题】溶液、浊液与溶解度;金属与金属材料.
【分析】A.根据铁锈的结构来分析;
B.根据洗涤剂具有乳化功能分析;
C.根据防锈的方法来分析;
D.根据氧化铝的特性考虑.
【解答】解:A.铁锈是一种疏松多孔的物质,能够把水蒸气和氧气保留在钢铁制品的表面,从而促进钢铁制品生锈,故错误;
B.洗涤剂具有乳化功能,所以洗涤剂能洗掉油污,故正确;
C.钢铁生锈的条件是钢铁与氧气和水同时接触,用过的菜刀用抹布擦干防止生锈,故正确;
D.铝制品表面有一层致密的氧化铝薄膜,使里面的铝与空气隔绝,起到保护作用,如果用钢丝刷擦洗铝制品上的污垢,容易把氧化铝擦掉,起不到保护作用了,故正确.
故选A.
【点评】本题主要考查了日常生活中的一些做法的判断,通过该题,对一些操作不当的做法需要引起注意,加以修改.
下列有关金属的说法正确的是( )
A.铝元素在地壳中含量最多,使用也最早
B.不锈钢的抗腐蚀性强于纯铁,硬度小于纯铁
C.灯泡里的灯丝常用钨制成
D.地球上金属矿物资源储量有限,可再生
【考点】合金与合金的性质;金属的物理性质及用途;金属元素的存在及常见的金属矿物;地壳中元素的分布与含量.
【专题】化学知识生活化;金属与金属材料.
【分析】A、根据地壳中含量最多的元素是氧元素进行分析;
B、根据合金的特性进行分析;
C、根据钨的特性进行分析;
D、根据地球上金属矿物资源的现状进行分析.
【解答】解:A、地壳中含量最多的元素是氧元素,地壳中含量最多的金属元素是铝,铝的活动性比铁还强,难以炼制铝的单质,所以到近代才被大量应用,故A错误;
B、不锈钢属于铁的合金,不锈钢的抗腐蚀性强于纯铁,硬度大于纯铁,故B错误;
C、电灯泡里的灯丝常用钨制成,因为钨的熔点高,故C正确;
D、金属矿物储量是有限的,并且不能再生,故D错误;
故选C.
【点评】本题主要考查了有关金属的知识,完成此题,可以依据已有的知识进行.
下列化学方程式书写正确的是( )
A.2Fe+6HCl═2 Fe Cl3+3H2↑ B.C+2 CuO═CO2↑+2Cu
C.Cu+2AgNO3═Cu(NO3)2+2Ag D.Mg+O2![]()
![]() MgO2
MgO2
【考点】书写化学方程式.
【专题】元素与化合物;化学用语和质量守恒定律.
【分析】根据化学方程式判断正误的方法需考虑:应用的原理是否正确;化学式书写是否正确;是否配平;反应条件是否正确;↑和↓的标注是否正确.
【解答】解:A、铁和盐酸反应生成氯化亚铁和氢气,正确的化学方程式为:Fe+2HCl═FeCl2+H2↑.
B、该化学方程式缺少反应条件,正确的化学方程式应为C+2CuO![]()
![]() CO2↑+2Cu.
CO2↑+2Cu.
C、该化学方程式书写完全正确.
D、该化学方程式氧化镁的化学式书写错误,正确的化学方程式应为2Mg+O2![]()
![]() 2MgO.
2MgO.
故选:C.
【点评】本题难度不大,在解此类题时,首先分析应用的原理是否正确,然后再根据方程式的书写规则进行判断;化学方程式正误判断方法是:先看化学式是否正确,再看配平,再看反应条件,再看气体和沉淀,最后短线改成等号.
如图是a、b、c三种物质的溶解度曲线,下列分析不正确的是( )
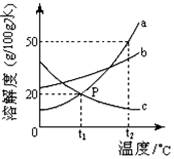

A.t2℃时a、b、c三种物质的溶解度由大到小的顺序是 a>b>c
B.t2℃时,将50g a物质放入100g水中充分溶解得到a的饱和溶液(a物质不含结晶水)
C.将t2℃时a、b、c三种物质的饱和溶液降温至t1℃时,所得溶液的溶质质量分数关系是b>a=c
D.t1℃时a的饱和溶液的溶质质量分数为16.7%
【考点】固体溶解度曲线及其作用;溶质的质量分数、溶解性和溶解度的关系.
【专题】溶液、浊液与溶解度.
【分析】根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
【解答】解:A、通过分析溶解度曲线可知,t2℃时a、b、c三种物质的溶解度由大到小的顺序是:a>b>c,故A正确;
B、t2℃时,a物质的溶解度是50g,所以将50ga物质放入100g水中充分溶解得到a的饱和溶液,故B正确;
C、t1℃时,b物质的溶解度最大,a物质次之,a、b物质的溶解度随温度的降低而减小,会析出晶体,c物质的降低温度,不会析出晶体,应该按照t2℃时进行计算,所以将t2℃时a、b、c三种物质的饱和溶液降温至t1℃时,所得溶液的溶质质量分数关系是b>a>c,故C错误;
D、t1℃时a物质的溶解度是20g,所以饱和溶液的溶质质量分数为:![]()
![]() ×100%=16.7%,故D正确.
×100%=16.7%,故D正确.
故选:C.
【点评】本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.
本卷还有8题,登录并加入会员即可免费使用哦~

该作品由: 用户张硕分享上传
可圈可点是一个信息分享及获取的平台。不确保部分用户上传资料的来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系 可圈可点 ,我们核实后将及时进行处理。