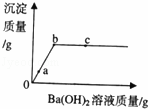
向一定量的硫酸铜溶液中加入一定质量分数的氢氧化钡溶液,直至过量.生成沉淀的质量与加入氢氧化钡溶液的质量关系如图所示,下列说法中正确的是( )
|
| A. | 0﹣a段只生成氢氧化铜沉淀 |
|
| B. | 室温下,b点溶液的pH>7 |
|
| C. | c点溶液中溶质至少有两种 |
|
| D. | 整个过程中,溶液中氢元素的质量一直在增加 |
考点:
盐的化学性质;溶液的酸碱性与pH值的关系.
专题:
常见的盐 化学肥料.
分析:
A、O至a段硫酸铜与氢氧化钡溶液反应生成氢氧化铜和硫酸钡沉淀;
B、b点表示两物质恰好反应;
C、根据c点表示氢氧化钡过量来分析;
D、根据溶液中溶剂为水来分析.
解答:
解:A、O至a段硫酸铜与氢氧化钠溶液反应生成氢氧化铜和硫酸钡两种沉淀;故错误;
B、b点时,两者恰好完全反应,故对应的液体中只有水一种,pH=7,故错误;
C、c点时,氢氧化钡溶液有剩余,故c点溶液中溶质只有氢氧化钡,故错误;
D、因为氢氧化钡溶液中含有水,水中有氢元素,故整个过程中,溶液中氢元素的质量一直在增加,故D正确;
故选D
点评:
本题重点考查复分解反应的实质,学会分析图象,判断产物,属于一道溶液综合性的题目.
波尔多液是一种农业上常用的杀虫剂,它由硫酸铜、生石灰加水配制而成.
(1)硫酸铜所含阴离子的符号是 .生石灰加水过程中会 (填“放”或“吸”)热
(2)煅烧石灰石(主要成分CaCO3)可制得生石灰(CaO).若要制取11.2t氧化钙,根据化学方程式计算需要碳酸钙的质量是多少?
(3)波尔多液不能用铁质容器来配制的原因是. .
考点:
盐的化学性质;生石灰的性质与用途;物质发生化学变化时的能量变化;书写化学方程式、文字表达式、电离方程式;根据化学反应方程式的计算.
专题:
常见的盐 化学肥料.
分析:
(1)根据硫酸铜在溶液中会电离出铜离子和硫酸根离子,氧化钙和水反应生成氢氧化钙,放出热量进行分析;
(2)根据碳酸钙在高温的条件下生成氧化钙和二氧化碳,然后结合题中的数据进行解答;
(3)根据铁和硫酸铜反应生成硫酸亚铁和铜进行分析.
解答:
解:(1)硫酸铜在溶液中会电离出铜离子和硫酸根离子,所以硫酸铜所含阴离子的符号是S![]() ,氧化钙和水反应生成氢氧化钙,放出热量;
,氧化钙和水反应生成氢氧化钙,放出热量;
(2)设需要碳酸钙质量为x,
CaCO3![]() CaO+CO2↑
CaO+CO2↑
100 56
x 11.2t
![]() =
=![]()
x=20t;
(3)铁和硫酸铜反应生成硫酸亚铁和铜,化学方程式为:Fe+CuSO4═FeSO4+Cu.
故答案为:(1)S![]() ,放;
,放;
(2)20t;
(3)Fe+CuSO4═FeSO4+Cu.
点评:
本题主要考查了和波尔多液有关的化学知识,难度不大,需要加强识记.
“比较归纳法”是学习化学的一种重要方法.(“﹣”表示相连的两种物质能发生反应,“﹣”表示某种物质可通过一步反应转化为另一种物质.)
(1)请以表2中序号Ⅰ为示例,填写序号Ⅱ、Ⅲ中的空格:
| 项目 序号 | 举例 | 物质类别间的相互反应 | 物质类别间的相互转化 |
| Ⅰ | CaCl2+Na2CO3=CaCO3↓+2NaCl2 | 盐1﹣盐2 | 盐→新盐 |
| Ⅱ | 写出硫酸与氯化钡反应的化学方程式 | 酸﹣盐 | 酸→ |
| Ⅲ | 写出氢氧化钠转变成另一种碱的 | 碱﹣ | 碱→新碱 |
(2)室温下,氯化镁与下列物质的变化关系,正确的是 (填标号).
A.MgCl2﹣AgN03
B.KN03﹣MgCl2
C.MgCl2﹣HCl
D.Mg(OH)2﹣MgCl2.
考点:
盐的化学性质;书写化学方程式、文字表达式、电离方程式.
专题:
常见的盐 化学肥料.
分析:
(1)氯化钡和稀硫酸反应生成硫酸钡沉淀和氯化氢;氢氧化钠溶液和硫酸铜溶液反应生成氢氧化铜沉淀和硫酸钠,
解答:
解:(1)氯化钡和稀硫酸反应的化学方程式为:BaCl2+H2SO4═BaSO4↓+2HCl.酸与盐反应生成新酸和新盐;
故填:BaCl2+H2SO4═BaSO4↓+2HCl;新酸;
氢氧化钠溶液和硫酸铜溶液反应生成氢氧化铜沉淀和硫酸钠,反应的化学方程式为:2NaOH+CuSO4=Na2SO4+Cu(OH)2↓;碱与盐反应生成新碱和新盐
故填:2NaOH+CuSO4=Na2SO4+Cu(OH)2↓;盐.
(2)MgCl2+AgN03=AgCl↓+Mg(N03)2;故A正确;
KN03既不与MgCl2反应也不能通过化学反应转化为MgCl2,故B不正确;+2H2O
MgCl2既不与HCl反应也不能通过化学反应转化为HCl,故C不正确;
Mg(OH)2+2HCl=MgCl2+2H2O,故D正确;
故选:AD.
点评:
书写化学方程式要注意四步:一是反应物和生成物的化学式要正确;二是要遵循质量守恒定律,即配平;三是要有必要的条件;四是看是否需要“↑”或“↓”.
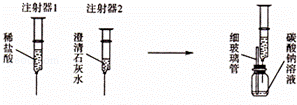
碳酸钠与盐酸的反应是分两步进行的,第一步反应的化学方程式为:Na2CO3+HCl═NaCl+NaHCO3.为验证该反应分两步进行.如图所示进行实验(装置气密性良好).
步骤Ⅰ:用注射器1向小药瓶中緩慢注入一定量的稀盐酸,边注入边振蕩,细玻璃管中液柱略微升高;換注射器2从瓶中缓慢抽取气体,澄清石灰水不浑浊.
步骤Ⅱ:…
(1)补充步骤Ⅱ的实验操作和预期现象.
(2)说明细玻璃管在实验中的作用.
(3)实验后,将小药瓶、注时器1、注射器2中的所有物质依次倒入一个洁净的烧杯中,只得到无色溶液,向其中滴加酚酞溶液不变色.写出溶液中溶质成分存在的几种情况(酚酞省略不写).
考点:
盐的化学性质.
专题:
常见的盐 化学肥料.
分析:
(1)根据过量的稀盐酸会和碳酸氢钠反应产生二氧化碳,二氧化碳能够使澄清的石灰水变浑浊回答;
(2)根据瓶内的气压变化会产生的影响分析作用;
(3)根据滴加酚酞的实验现象及反应的程度、反应的产物分析.
解答:
解:(1)因为少量的盐酸会和碳酸钠反应产生碳酸氢钠,不会产生二氧化碳,因此石灰水无明显变化;可以继续加稀盐酸,稀盐酸会和碳酸氢钠反应产生二氧化碳,二氧化碳能够使澄清的石灰水变浑浊;故答案为:换注射器1向小药瓶中继续注入稀盐酸,至较多气泡产生,细玻璃管中液柱明显升高,换注射器2从瓶中缓慢抽取气体,澄清石灰水变浑浊;
(2)由于反应产生大量的二氧化碳可能会产生过大的气压,会把瓶塞弹出,细玻璃管与大气相连,瓶内的气体会把部分液体压入玻璃管内,从而起到缓冲的作用,也可以通过液柱的上升,说明有气体的生成;故答案为:细玻璃管调节小药瓶内的气压,防止瓶内气压过大时瓶塞弹出;显示小药瓶内、外的压强差,帮助判断瓶中是否有气体生成;
((3)因为盐酸会和碳酸钠反应产生氯化钠和水、二氧化碳;实验后,将小药瓶、注时器1、注射器2中的所有物质依次倒入一个洁净的烧杯中,二氧化碳和氢氧化钙反应产生的碳酸钙沉淀,而只得到无色溶液,说明碳酸钙和盐酸反应产生氯化钙、水和二氧化碳,向其中滴加酚酞溶液不变色,说明没有碱性物质的存在,但可能是酸性物质盐酸的过量,故答案为:氯化钠、氯化钙;氯化钠、氯化钙、氯化氢.
点评:
本题属于信息题的考查,能够根据题目的信息结合物质的性质进行模拟设计实验、描述实验现象、得出实验结论是解题的关键,难度较大.
某同学对含有泥沙的粗盐进行提纯,并用提纯后的氯化钠配制100g质量分数为5%的氯化钠溶液.请回答有关问题:
(1)按下面步骤提纯粗盐:
①取一定质量的粗盐样品,加水溶解;②通过 操作将泥沙除去;③将滤液移入蒸发皿,蒸发结晶,得到氯化钠晶体.
(2)在上述实验步骤中,都使用了同一仪器 (填名称),它在步骤①和③的操作方法相同,但目的不同,步骤①的目的是 ,步骤③的目的是 ;
(3)利用上述实验得到的氯化钠晶体,配制100g质量分数为5%的氯化钠溶液:
①配制溶液的步骤:计算、 溶解、装瓶;
②量取所需的水应选用 mL的量筒.
考点:
氯化钠与粗盐提纯;一定溶质质量分数的溶液的配制.
专题:
溶液、浊液与溶解度;常见的盐 化学肥料.
分析:
(1)粗盐的主要成分是氯化钠,根据氯化钠易溶于水、泥沙等杂质难溶于水,进行分析解答.
(2)根据溶解、过滤、蒸发操作所需的仪器,进行分析解答.
(3)①根据配制溶质质量分数一定的溶液的基本步骤进行分析解答.
②利用溶质质量=溶液质量×溶质的质量分数,溶剂质量=溶液质量﹣溶质质量,根据溶液的质量和溶质的质量分数,计算配制溶液所需要的水的质量;进而由所需水的体积判断所需量筒的量程.
解答:
解:(1)粗盐的主要成分是氯化钠,氯化钠易溶于水、泥沙等杂质难溶于水,取一定质量的粗盐样品,加水溶解,使不溶物与食盐初步分离→过滤(把泥沙除去)→将滤液移入蒸发皿,蒸发结晶,得到氯化钠晶体蒸发.
(2)溶解、过滤、蒸发操作中都要用到的实验仪器是玻璃棒,它在步骤①溶解和③蒸发的操作方法相同,但目的不同,①溶解中作用是搅拌,加快食盐的溶解速率,③蒸发的作用是搅拌,防止滤液飞溅.
(3)①配制100g质量分数为5%的氯化钠溶液,首先计算配制溶液所需氯化钠和水的质量,再称量所需的氯化钠和量取水,最后进行溶解、装瓶.
②溶质质量=溶液质量×溶质的质量分数,配制100g质量分数为5%的氯化钠溶液,需氯化钠的质量=100g×5%=5g;溶剂质量=溶液质量﹣溶质质量,则所需水的质量=100g﹣5g=95g(合95mL),应选用100mL的量筒.
故答案为:(1)过滤;(2)玻璃棒;搅拌,加快食盐的溶解速率;搅拌,防止滤液飞溅;(3)①称量;②100.
点评:
本题难度不大,掌握粗盐提纯的原理、实验步骤(溶解、过滤、蒸发)、所需的仪器、配制溶质质量分数一定的溶液的基本步骤等是正确解答本题的关键.
本卷还有28题,登录并加入会员即可免费使用哦~

该作品由: 用户朱丰胜分享上传
可圈可点是一个信息分享及获取的平台。不确保部分用户上传资料的来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系 可圈可点 ,我们核实后将及时进行处理。