下列关于水的净化,正确的是
A .活性炭的吸附性属于化学性质 B .过滤可以除去所有杂质
C .明矾净水的作用是杀菌消毒 D .蒸馏对水的净化程度最高
D
【详解】 A 、活性炭吸附过程中没有新物质生成,属于物理变化,吸附性属于物理性质,故说法错误;
B 、过滤适用于不溶于水的固体和液体,只能除去不溶性杂质,不能除去可溶性杂质,故说法错误;
C 、明矾溶于水形成的胶体能将不溶性固体小颗粒凝聚在其表面,可以加速沉降,不能杀菌消毒,故说法错误;
D 、蒸馏是通过加热的方法使水沸腾变成水蒸气 , 然后冷凝成水的过程,是净化程度最高的一种方法,故说法正确;
故选 D 。
如图是我们学过的蒸馏装置,关于蒸馏实验说法不正确的是
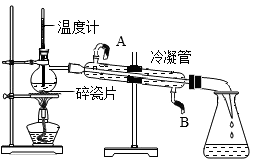
A .加热蒸馏烧瓶必须垫石棉网 B .图中冷凝水的流动方向是 A→B
C .温度计应该放在蒸馏烧瓶的支管口,测气体温度 D .烧瓶中碎瓷片的作用是防止液体暴沸
B
【详解】 A 、蒸馏烧瓶不能直接加热,因此加热蒸馏烧瓶必须垫石棉网 ,故 A 正确;
B 、实验时,以保证水充满冷凝管,起到充分冷凝,冷凝管应适当倾斜,冷凝管应从下口进水,上口出水,故其进、出水的方向是 B 进 A 出,即图中冷凝水的流动方向是 B→A ,故 B 不正确;
C 、温度计在实验中经常使用,图中位置错误,水银球不能插入液态水中温度计水银球在蒸馏烧瓶支管口处,故 C 正确;
D 、在蒸馏烧瓶中加碎瓷片的作用是防止暴沸,故 D 正确;
故选 B 。
茶艺是一种文化、更是一种生活艺术。泡茶时。茶壶中的滤网将茶水与茶叶分离。下列实验操作与这种分离方法原理相似的是
A .溶解 B .蒸发 C .过滤 D .蒸馏
C
【详解】 A 、溶解是将液体、固体或气体分散在液体中,不符合题意;
B 、蒸发是物质从液态转化为气态的过程,不符合题意;
C 、过滤是指通过粒径的差异将固液混合物中的固体和液体分离出来,泡茶时,茶叶片径远大于水的粒径,倒茶时,因为重力作用使得水可以通过滤网,茶叶则被滤网截留,其类似于过滤操作,符合题意;
D 、蒸馏是利用混合液体或液 - 固体系中各组分沸点不同,使低沸点组分蒸发,再冷凝以分离整个组分的操作过程,不符合题意。
故选 C 。
实验安全重中之重,下列做法符合安全操作规程的是
A . 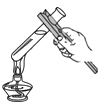 加热足量的液体 B .
加热足量的液体 B . 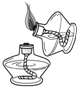 点燃另一盏酒精灯
点燃另一盏酒精灯
C . 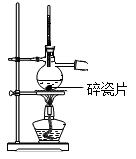 蒸馏时加几粒碎瓷片 D .
蒸馏时加几粒碎瓷片 D .  凑到瓶口闻气味
凑到瓶口闻气味
C
【详解】 A 、给试管中的液体加热时,应用外焰加热,且试管里的液体不能超过试管容积的 1/3 ,图中试管中的液体超过试管容积的 1/3 ,不符合题意;
B 、禁止用燃着的酒精灯去点燃另一只酒精灯,防止发生火灾,不符合题意;
C 、蒸馏时,加几粒碎瓷片,可以防止暴沸,符合题意;
D 、闻气味时,应用手在瓶口轻轻扇动,使少量气味飘进鼻孔中,不能凑到瓶口去闻,不符合题意。
故选 C 。
下列说法正确的数量是
① 煤加工的产物包括煤焦油、煤气、焦炭和粗氨水等
② 蒸馏也可以起到消毒杀菌的作用
③ 用熟石灰可以鉴别氮肥和钾肥
④ 与酸反应生成盐和水的物质只有碱、碳酸盐和碳酸氢盐
⑤ 有一包不纯的碳酸钾粉末,所含杂质可能是硝酸钾、硝酸钙、氯化钾、氯化铁、碳酸钠中的一种或几种。为确定其成分,取 13.8g 该粉末于试管中,加足量的水充分溶解,得到无色澄清溶液。向该溶液中加入适量的硝酸银溶液,恰好完全反应,产生白色沉淀 27.6g ,再加入足量的稀硝酸,充分反应后,沉淀全部消失,该包粉末中一定含有碳酸钾、碳酸钠,可能含有硝酸钾。
A . 1 个 B . 2 个 C . 3 个 D . 4 个
B
【详解】 ① 煤加工的产物包括煤焦油、煤气、焦炭和粗氨水等,正确;
② 蒸馏的原理是将沸点相差较大的液态混合物加热使沸点低的物质先汽化,再使其液化的连续操作过程,属于物理变化,但是水的蒸馏通过加热的方法使水变成水蒸气后冷凝成水,除去了可溶性杂质也可以杀死水中的细菌,故蒸馏也可以起到消毒杀菌的作用,正确;
③ 铵态氮肥才能与熟石灰反应放出氨气,尿素属于氮肥,不属于铵态氮肥,不能与熟石灰反应释放出氨气,钾肥也不能与熟石灰反应放出氨气,所以用熟石灰不一定可以鉴别氮肥和钾肥,错误;
④ 与酸反应生成盐和水的物质有碱、碳酸盐和碳酸氢盐,还有金属氧化物,错误;
⑤ 有一包不纯的碳酸钾粉末,所含杂质可能是硝酸钾、硝酸钙、氯化钾、氯化铁、碳酸钠中的一种或几种。为确定其成分,取 13.8g 该粉末于试管中,加足量的水充分溶解,得到无色澄清溶液。氯化铁在溶液中显黄色,故一定不含氯化铁,硝酸钙与碳酸钠或碳酸钾反应会生成碳酸钙沉淀,故一定不含有硝酸钙,向该溶液中加入适量的硝酸银溶液,恰好完全反应,产生白色沉淀 27.6g ,再加入足量的稀硝酸,充分反应后,沉淀全部消失,碳酸根离子与阴离子生成碳酸银沉淀,氯离子与银离子生成氯化银沉淀,由于沉淀完全消失,故一定不含有氯化钾,设 13.8g 全部是碳酸钾,根据碳酸根离子守恒,则生成碳酸银沉淀的质量为 x ,
,解得 x =27.6g ,若全部是碳酸钠,根据碳酸根离子守恒,由于碳酸钠的相对分子质量为 106 小于 138 ,故生成沉淀的质量大于 27.6g ,故根据极值法确定必须有产生碳酸银沉淀较少的或者不产生沉淀的物质与产生碳酸银沉淀较多的物质混合,故碳酸钾中必须混有碳酸钠和硝酸钾,也可以生成 27.6g 碳酸银沉淀,故该包粉末中一定含有碳酸钾、碳酸钠、硝酸钾,一定不含有氯化铁、氯化钾、硝酸钙;错误;
共有 2 个正确的,故选 B 。
本卷还有30题,登录并加入会员即可免费使用哦~

该作品由: 用户郑曲路分享上传
可圈可点是一个信息分享及获取的平台。不确保部分用户上传资料的来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系 可圈可点 ,我们核实后将及时进行处理。