根据下列实验操作和现象所得到的结论正确的是 ( )
| 选项 | 实验操作和现象 | 实验结论 |
| A | 将燃着的硫放入充满 O 2 的集气瓶里,硫继续燃烧发出蓝紫色火焰,同时产生有刺激性气味的气体 | 硫与氧气发生化学反应生成 SO 2 |
| B | 将黄铜片 ( 铜锌合金 ) 和铜片互相刻划,发现铜片表面留下的刻度更为明显 | 合金的硬度比组成它们的纯金属更高 |
| C | 将某可燃物置于足量的 O 2 中点燃,充分燃烧后,检验测到有 H 2 O 和 CO 2 生成 | 该可燃物由 C 、 H 两种元素组成 |
| D | 将一洁净无绣的铁钉浸没在蒸馏水中,一段时间后铁钉表面锈蚀 | 铁生锈的主要条件是与空气和水直接接触 |
A . A B . B C . C D . D
AB
【详解】
A 、硫和氧气反应生成二氧化硫,故 A 正确;
B 、铜片是纯金属,留下划痕说明硬度小,合金比组成它们的纯金属硬度大,故 B 正确;
C 、生成物有水和二氧化碳,根据质量守恒定律,反应物中一定有碳、氢两种元素,但是反应物中氧元素可能有,故 C 错误;
D 、洁净的铁钉浸没在蒸馏水中生锈,不能说明铁生锈的主要条件是与空气和水直接接触,故 D 错误。
故选 AB
化学概念间的逻辑上有如图所示的部分关系,对下列概念间的关系说法正确的是( )
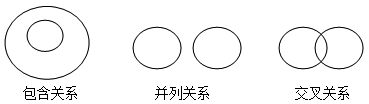
A . 纯净物与混合物属于交叉关系
B . 氧气与混合物属于交叉关系
C . 空气和混合物属于包含关系
D . 氧化反应与化合反应属于并列关系
C
【详解】
A 、 物质分为纯净物、混合物,纯净物与混合物属于并列关系,错误;
B 、 氧气是一种物质,属于纯净物;混合物是多种物质组成的,两者不是交叉关系,错误;
C 、 空气是多种物质组成的混合物;所以空气和混合物属于包含关系,正确;
D 、 氧化反应可能是化合反应,也可能不是化合反应,化合反应可能是氧化反应,也可能不是氧化反应,氧化反应与化合反应属于交叉列关系,错误。
故选 C 。
下列关于物质在氧气中燃烧的现象错误的是( )
A . 硫粉在氧气中燃烧,产生蓝紫色火焰,放热,产生刺激性气味的气体
B . 铁丝在氧气中剧烈燃烧,火星四溅,产生黑色固体
C . 木炭在氧气中燃烧,发白光,放热,产生二氧化碳
D . 红磷在氧气中燃烧,发黄光,冒白烟,产生大量的热
C
【详解】
A 、硫粉在氧气中燃烧生成明亮的蓝紫色火焰,同时释放大量的热量,生成刺激性气味的气体,描述的实验正确,不符合题意;
B 、铁丝在氧气中剧烈燃烧,火星四射同时释放出大量的热量,生成黑色固体,描述的实验正确,不符合题意;
C 、木炭在氧气中燃烧发出白光同时释放大量的热量, “产生二氧化碳气体” 是描述的实验结论,不是实验现象,描述的实验错误,符合题意;
D 、红磷在氧气中燃烧,发黄光,冒白烟,产生大量的热,描述的实验正确,不符合题意。
故选 C 。
下列说法中不正确的是( )
A . 木炭在空气中燃烧发出红色的火焰,生成的气体能使澄清的石灰水变浑浊
B . 红热的铁丝伸入氧气中剧烈燃烧,火星四射,生成黑色固体
C . 硫粉在氧气中燃烧产生明亮蓝紫色火焰
D . 红磷点燃后伸入氧气中产生大量白烟
A
【分析】
A 、根据木炭在空气中燃烧的现象进行分析判断。 B 、根据铁丝在氧气中燃烧的现象进行分析判断。 C 、根据硫在氧气中燃烧的现象进行分析判断。 D 、根据红磷在氧气中燃烧的现象进行分析判断。
【详解】
A 、木炭在空气中燃烧发出红光,生成的气体能使澄清的石灰水变浑浊,选项说法错误;
B 、红热的铁丝伸入氧气中剧烈燃烧,火星四射,生成黑色固体,选项说法正确;
C 、硫粉在氧气中燃烧产生明亮蓝紫色火焰,选项说法正确;
D 、红磷点燃后伸入氧气中产生大量白烟,选项说法正确;
下列实验现象的描述中,正确的是( )
A . 镁带在空气中燃烧,发出耀眼的白光,放热,生成白色粉末
B . 硫在氧气中燃烧,发出淡蓝色火焰,闻到刺激性气味
C . 白磷和红磷在空气中燃烧,都产生大量的白雾,放出热量
D . 铁丝在空气中燃烧,火星四溅,生成四氧化三铁
A
【分析】
A 、根据镁带在空气中燃烧的现象进行分析判断;
B 、根据硫在氧气中燃烧的现象进行分析判断;
C 、根据白磷和红磷在空气中燃烧的现象进行分析判断;
D 、根据铁丝在空气中不能燃烧,进行分析判断。
【详解】
A 镁带在空气中燃烧,发出耀眼的白光,放热,生成一种白色粉末,故选项说法正确.
B 、硫在氧气中燃烧,发出明亮的蓝紫色火焰,产生一种具有刺激性气味的气体,故选项说法错误.
C 、白磷和红磷在空气中燃烧,产生大量的白烟,而不是白雾,故选项说法错误.
D 、铁丝在空气中只能烧至发红,不会剧烈燃烧、火星四射,故选项说法错误。
本卷还有95题,登录并加入会员即可免费使用哦~

该作品由: 用户尹沫辰分享上传
可圈可点是一个信息分享及获取的平台。不确保部分用户上传资料的来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系 可圈可点 ,我们核实后将及时进行处理。