鸡蛋壳的主要成分是碳酸钙(其他成分不溶于水也不与酸反应)。化学兴趣小组为了测定鸡蛋壳中碳酸钙的含量,做如下实验:
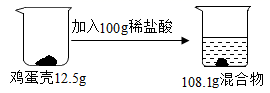
反应结束后,发现溶液呈酸性,为防止溶液腐蚀下水管道,过滤后向滤液中加入一定量的 Ca(OH) 2 固体粉末至中性,蒸发溶液得固体 33.3g 。
( 1 )该鸡蛋壳中碳酸钙的质量为多少 ? (写出计算过程)
( 2 )稀盐酸的溶质质量分数 ___________ 。
答案
( 1 )依据质量守恒定律,生成 CO 2 的质量为 100g+12.5g-108.1g=4.4g
设鸡蛋壳中碳酸钙的质量为 x ,反应的盐酸的质量为 y ,生成的 CaCl 2 为 z 。
,解得 x =10g
,解得 y =7.3g
,解得 z =11.1g
答:该鸡蛋壳中碳酸钙的质量为 10g 。
( 2 ) 21.9%
【详解】
( 2 )反应结束后,溶液呈酸性,说明溶液中还含有 HCl ,故滤液中的溶质为 CaCl 2 和 HCl 。向滤液中加入一定量的 Ca(OH) 2 固体粉末至中性,蒸发溶液得到的固体为 HCl 与 Ca(OH) 2 反应生成的 CaCl 2 和滤液中的 CaCl 2 , HCl 与 Ca(OH) 2 反应生成的 CaCl 2 质量为 33.3g-11.1g=22.2g 。
设与 Ca(OH) 2 反应的 HCl 的质量为 a 。
解得 a =14.6g
参与反应的稀盐酸的质量为 7.3g+14.6g=21.9g 。
稀盐酸的溶质质量分数为 × 100%=21.9% 。



 五氧化二磷
五氧化二磷