实验小组探究盐酸和氢氧化钠反应过程中溶液 pH 的变化规律,得到如图所示曲线。下列有关该实验事实的说法正确的是
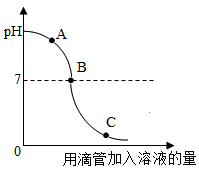
A .该实验是将氢氧化钠溶液滴入盐酸中
B . B 点表示盐酸和氢氧化钠恰好完全反应
C . A 点时的溶液能使酚酞试液变红
D . C 点时,溶液中的溶质只有氯化钠
答案
BC
【详解】
A 、通过图示可知,溶液初始状态的 pH > 7 ,则溶液中应该盛放的是氢氧化钠溶液,该实验是向氢氧化钠溶液中逐滴滴加稀盐酸。 A 错误;
B 、 B 点的 pH=7 ,则证明此时,盐酸和氢氧化钠恰好完全反应,生成氯化钠和水,溶液呈中性。 B 正确;
C 、 A 点的 pH > 7 ,溶液呈碱性。碱性溶液能使无色酚酞变红。 C 正确;
D 、 C 点的 pH < 7 ,溶液显酸性。则此时溶液中的溶质除了有生成的氯化钠,还有过量的氯化氢。 D 错误。
故选 BC 。