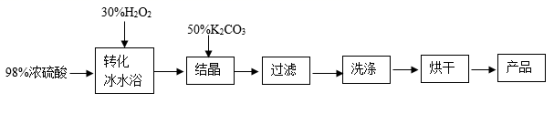
过硫酸氢钾复盐( K 2 SO 4 ·KHSO 4 ·2KHSO 5 ) 易分解,易溶于水,可用作漂白剂、 NO x 、 SO 2 等废气脱除剂。某研究小组制备过硫酸氢钾复盐的流程如图:
( 1 )已知 H 2 O 2 ,受热易分解,请写出化学方程式 _____ 。
( 2 )在 “ 转化 ” 操作前,需先用冰水冷却双氧水,可能的原因是 _____“ 转 ” 化 ” 过程中,浓硫酸与 H 2 O 2 ,发生反应生成过硫酸( H 2 SO 5 ),写出该变化的化学反应方程式 _____ 。
( 3 )用无水乙醇取代蒸馏水洗涤沉淀,目的是 _____ 和便于干燥,烘干时用红外灯低于 40℃ ,可能的原因是 _____ 。
( 4 )过硫酸氢钾复盐产率(以产品含氧量表示)随溶液 pH 和温度的变化关系如图所示。则该过程适宜的条件是 _____ 。
答案
过氧化氢受热易分解
洗掉晶体表面杂质 产品在 40℃ 以上易分解 0℃ 、 pH=2 左右
【详解】
(1) 过氧化氢受热易分解其化学方程式为: ;
(2) 浓硫酸与 H 2 O 2 溶液混合时,大量放热,温度高, H 2 O 2 易分解,故在 “ 转化 ” 中,用冰水冷却双氧水;浓硫酸与 H 2 O 2 反应,部分转化为过硫酸 H 2 SO 5 和水,反应为: 故 ② 答案为:过氧化氢受热易分解;
(3) 无水乙醇洗涤沉淀,可以洗除晶体表面的杂质,同时乙醇易挥发,便于晶体干燥;过硫酸氢钾复盐( K 2 SO 4 •KHSO 4 •2KHSO 5 )易分解,则烘干产品时,用红外灯低于 40℃ 烘干,可能的原因是产品在 40℃ 以上易分解;故答案为:洗掉晶体表面杂质、产品在 40℃ 以上易分解;
(4) 根据图示, 0℃ 、 pH=2 左右时,过硫酸氢钾复盐产率(以产品含量氧表示)最大,故此条件为最适宜条件;故答案为: 0℃ 、 pH=2 左右。

 CO2是碳充分燃烧的化学方程式。
CO2是碳充分燃烧的化学方程式。  2H2↑+O2↑为例加以说明。
2H2↑+O2↑为例加以说明。 