用作牙膏摩擦剂的轻质碳酸钙可以用矿石 来制备,某化学兴趣小组设计了
种转化流程,如图所示.
(生产流程)

(相关资料)
a .二氧化碳持续通入氢氧化钙溶液发生如下反应:
,
;
b .碳酸氢钙微溶于水,微热易分解: ;
c .生石灰与水充分反应后可得到颗粒非常细小的熟石灰浆.
(问题讨论)
小王主张用流程 ① 、 ② 、 ④ 和操作
的设计.请写出反应 ① 和 ④ 的化学方程式:
①________ ; ④________ ;
操作 包括搅拌和 ________ 、洗涤、烘干等工序;该流程中,通过反应 ④ 可回收副产品 _____ .
小李认为流程 ① 、 ② 、 ③ 和操作
比小王的主张更好,理由是: ________ ;
制轻质碳酸钙时,
为 ________ (选填 “ 悬浊液 ” 或 “ 溶液 ” ),理由是: ________ .
小李认为得到的产品中可能含有杂质
,所以操作
包括搅拌、 ________ 和过滤、烘干等工序,以提高产率.
(产品含量测定) 含量的测定:取
产品,研成粉状后,按图进行实验.
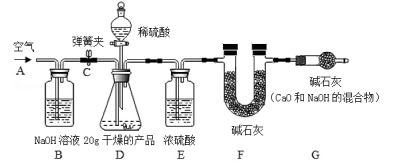
实验步骤:
① 连接好装置,检查气密性; ② 打开弹簧夹 ,在
处缓缓通入一段时间空气;
③ 称量 的质量; ④ 关闭弹簧夹
,慢慢滴加稀硫酸至过量,直至
中无气泡冒出;
⑤ 打开弹簧夹 ,再次缓缓通一段时间空气; ⑥ 称量
的质量,得前后两次质量差为
.
问题探究
① 产品研成粉的目的 ________ ;
② 装置的作用是 ________ ;
装置的作用是 ________ ,
③ 若没有 装置,则测定的
的质量分数会 ________ (填 “ 偏大 ” 、 “ 偏小 ” 、 “ 不变 ” ).
称量 的质量,得前后两次质量差为
,可求得产品中
的质量分数为 ________
.
(总结反思)
某同学设计上述实验方案测定牙膏中钙元素的质量分数:向一定量牙膏中加入过量稀盐酸,测定生成 的质量,据此计算牙膏中钙元素的质量分数.小李同学认为即使排除实验仪器和操作的影响,上述测定的结果仍不一定准确,理由是 ________ .
答案
CaCO 3 ![]() CaO+CO 2 ↑ Ca ( OH ) 2 +Na 2 CO 3 =CaCO 3 ↓+2NaOH 过滤 NaOH 二氧化碳得到充分利用,节约原料 悬浊液 澄清石灰水中氢氧化钙浓度太小,生产效率很低 微热 增大接触面积,充分反应; 除去空气中的二氧化碳, 防止空气中的二氧化碳进入
CaO+CO 2 ↑ Ca ( OH ) 2 +Na 2 CO 3 =CaCO 3 ↓+2NaOH 过滤 NaOH 二氧化碳得到充分利用,节约原料 悬浊液 澄清石灰水中氢氧化钙浓度太小,生产效率很低 微热 增大接触面积,充分反应; 除去空气中的二氧化碳, 防止空气中的二氧化碳进入 装置; 偏大,
; 二氧化碳能溶于水
【分析】
( 1 )碳酸钙能分解生成氧化钙,氧化钙能与水反应生成氢氧化钙,氢氧化钙能与二氧化碳或碳酸钠反应生成碳酸钙,生成的碳酸钙不溶于水,可以通过过滤的方法从溶液中分离出来;( 2 )根据物质的循环利用分析;( 3 )根据氢氧化钙的溶解性分析;( 4 )根据题中信息二氧化碳过量会生成碳酸氢钙以及碳酸氢钙微热分解的性质分析;( 6 )根据流程图及实验原理,要测定碳酸钙的质量分数,可测定生成的二氧化碳的质量,可利用 F 装置吸收二氧化碳,在吸收之前需除去二氧化碳中的水分及空气中的二氧化碳,因此要利用除去二氧化碳的空气将生成的二氧化碳全部排到 F 装置中,根据二氧化碳的溶解性解答。
【详解】
( 1 ) ① 碳酸钙高温分解生成氧化钙和二氧化碳,反应的化学方程式为 CaCO 3 ![]() CaO+CO 2 ↑ ; ④ 氢氧化钙能与碳酸钠发生复分解反应生成碳酸钙和氢氧化钠,生成的碳酸钙不溶于水,反应的化学方程式为 Ca ( OH ) 2 +Na 2 CO 3 =CaCO 3 ↓+2NaOH ;操作 Ⅱ 搅拌和过滤、洗涤、烘干等工序;该流程中,通过反应 ④ 可回收副产品 NaOH ;( 2 )流程 ① 、 ② 、 ③ 的 ③ 是将碳酸钙分解生成的二氧化碳加以利用,节约了原料;( 3 )制轻质碳酸钙时, D 为悬浊液,理由是:澄清石灰水中氢氧化钙浓度太小,生产效率很低;( 4 )由题中信息二氧化碳持续通入氢氧化钙溶液发生如下反应: CO 2 +Ca ( OH ) 2 =CaCO 3 ↓+H 2 O , CaCO 3 +H 2 O+CO 2 =Ca ( HCO 3 ) 2 ;碳酸氢钙微溶于水,微热易分解: Ca ( HCO 3 ) 2 ═CaCO 3 ↓+H 2 O+CO 2 ↑ 可知将碳酸氢钙转化成碳酸钙可以采用微热的方法;( 6 ) ① 增大接触面积,充分反应,可将产品研成粉末; ② 根据流程图装置分析,要通过测定生成的二氧化碳的质量计算碳酸钙的含量,则需将生成的二氧化碳用除去二氧化碳的空气全部排出,因此 B 装置的作用是除去空气中的二氧化碳; G 装置的作用是防止空气中的二氧化碳进入 F 装置; ③ 若没有 E 装置,生成的二氧化碳气体中含有水分而使二氧化碳的质量增大,则测定的 CaCO 3 的质量分数会偏大;称量 F 的质量,得前后两次质量差为 8.7g ,故生成的二氧化碳的质量为 8.7g 。
CaO+CO 2 ↑ ; ④ 氢氧化钙能与碳酸钠发生复分解反应生成碳酸钙和氢氧化钠,生成的碳酸钙不溶于水,反应的化学方程式为 Ca ( OH ) 2 +Na 2 CO 3 =CaCO 3 ↓+2NaOH ;操作 Ⅱ 搅拌和过滤、洗涤、烘干等工序;该流程中,通过反应 ④ 可回收副产品 NaOH ;( 2 )流程 ① 、 ② 、 ③ 的 ③ 是将碳酸钙分解生成的二氧化碳加以利用,节约了原料;( 3 )制轻质碳酸钙时, D 为悬浊液,理由是:澄清石灰水中氢氧化钙浓度太小,生产效率很低;( 4 )由题中信息二氧化碳持续通入氢氧化钙溶液发生如下反应: CO 2 +Ca ( OH ) 2 =CaCO 3 ↓+H 2 O , CaCO 3 +H 2 O+CO 2 =Ca ( HCO 3 ) 2 ;碳酸氢钙微溶于水,微热易分解: Ca ( HCO 3 ) 2 ═CaCO 3 ↓+H 2 O+CO 2 ↑ 可知将碳酸氢钙转化成碳酸钙可以采用微热的方法;( 6 ) ① 增大接触面积,充分反应,可将产品研成粉末; ② 根据流程图装置分析,要通过测定生成的二氧化碳的质量计算碳酸钙的含量,则需将生成的二氧化碳用除去二氧化碳的空气全部排出,因此 B 装置的作用是除去空气中的二氧化碳; G 装置的作用是防止空气中的二氧化碳进入 F 装置; ③ 若没有 E 装置,生成的二氧化碳气体中含有水分而使二氧化碳的质量增大,则测定的 CaCO 3 的质量分数会偏大;称量 F 的质量,得前后两次质量差为 8.7g ,故生成的二氧化碳的质量为 8.7g 。
设碳酸钙的质量为 x 。
CaCO 3 +2HCl═CaCl 2 +H 2 O+CO 2 ↑
100 44
x 8.7g
x=19.77g
故碳酸钙的质量分数为: ×100%=98.86%
【总结反思】理由是:二氧化碳能溶于水,而会使测得的二氧化碳体积偏小。

 CO2是碳充分燃烧的化学方程式。
CO2是碳充分燃烧的化学方程式。  2H2↑+O2↑为例加以说明。
2H2↑+O2↑为例加以说明。 