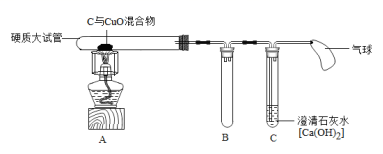
在实验室中,老师用下图所示的装置进行实验(夹持装置已省略):加热一段时间,反应正常进行,直到实验完成,停止加热并冷却到室温。
回答下列问题。
( 1 )硬质大试管中发生的化学反应方程式是 _________________ 。
( 2 )装置 A 产生的实验现象是 _______________________ , C 中产生的实验现象是 ____________________ 。
( 3 )酒精灯加网罩的作用是 ________________________ 。
( 4 )装置 B 的作用是 ___________________________ 。
( 5 )此套装置中气球的作用是 ________________________ 。
答案
固体由黑变红 澄清石灰水变浑浊 集中火焰,使局部温度升高 防止 C 中的液体倒流,炸裂试管 收集尾气
【详解】
( 1 )硬质大试管中发生的化学反应是碳与氧化铜在高温的条件下反应生成铜和二氧化碳,该反应的化学方程式是: ;
( 2 )氧化铜为黑色,铜为红色,装置 A 中产生的现象为:固体由黑变红;
反应生成的二氧化碳能使澄清石灰水变浑浊,故 C 中产生的实验现象是:澄清石灰水变浑浊;
( 3 )酒精灯加网罩的作用是:集中火焰,使局部温度升高;
( 4 )反应后,停止加热后,硬质大试管内温度降低,压强减小, C 中的液体会倒流,炸裂试管,故装置 B 的作用是:防止 C 中的液体倒流,炸裂试管;
( 5 )反应中炭粉过量,碳会与二氧化碳反应生成一氧化碳,一氧化碳有毒,会污染空气,故气球的作用是:收集尾气。

 Cu + H2O。
Cu + H2O。 
 H2O+Cu
H2O+Cu