某同学在学习木炭和氧化铜反应的知识后,产生了疑问:木炭与氧化铜反应生成的气体有哪些 ? 同学们带着疑问进行了下列探究:
【 提出猜想 】 猜想一:只有 CO 2 ;猜想二:只有 CO ;猜想三: _____ 。
【 查阅资料 】 没有磷钼酸溶液的氯化钯试纸遇二氧化碳无变化,但遇到微量一氧化碳会立即变成蓝色。
【 实验步骤 】 连接好实验装置,并进行实验,装置如下图所示(夹持仪器已省) :
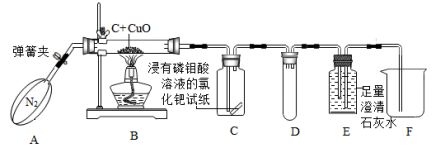
步骤一:实验前先通一段时间 N 2 ;步骤二:点燃酒精喷灯加热。
玻璃管中的现象是 _____ 。
【 实验结论 】
( 1 )若观察到氯化钯试纸不变色,澄清石灰水变浑浊,则猜想一成立, 请写出澄清石灰水变浑浊的化学方程式: _____ 。
( 2 )若观察到氯化钯试纸变蓝,澄清石灰水不变浑浊,则猜想 _____ 成立。
( 3 )若观察到氯化钯试纸 _____ ,澄清石灰水 _____ ,则猜想三成立。
【 实验反思 】
( 1 )该实验开始前通一会儿 N 2 的目的是: _____ 。
( 2 )有同学认为该装置需要添加尾气处理装置,你认为是否需要 ? 请说明理由。 _____ 。
答案
既有 CO 2 又有 CO 黑色粉末逐渐变为红色 二 变蓝 变浑浊 排尽装置内的空气,防止空气中的氧气对碳与氧化铜反应产物检验的干扰(答案合理即可) 不需要 ; 实验过程中产生的一氧化碳已收集在装置 E 中,没有排放到空气中,不会造成污染(答案合理即可)
【详解】
【 提出猜想 】
木炭粉与氧化铜反应生成物有三种可能: ① 气体产物全部是 CO 2 ; ② 气体产物全部是 CO ; ③ 气体产物是 CO 2 和 CO 的混合物;
【 实验步骤 】
玻璃管中氧化铜和碳反应生成铜和一氧化碳、二氧化碳,可观察到黑色粉末逐渐变为红色;
【 实验结论 】
( 1 )二氧化碳能使 C 中澄清的石灰水变浑浊,生成碳酸钙和水,反应的化学方程式为: ;
( 2 )若观察到氯化钯试纸变蓝说明有一氧化碳;澄清石灰水不变浑浊说明没有二氧化碳,则猜想二正确;
( 3 )因为浸有磷钼酸溶液的氯化钯试纸遇一氧化碳变量,若试纸变蓝,则有一氧化碳;如果澄清石灰水变浑浊,则有 CO 2 ,则猜想三成立;
【 实验反思 】
( 1 )实验中要排除空气的影响,故氮气的作用是排尽装置内的空气,防止空气中的氧气对碳与氧化铜反应产物检验的干扰(答案合理即可);
( 2 ) CO 有毒,是大气污染物,但本题不需要添加尾气处理装置,因为实验过程中产生的一氧化碳已收集在装置 E 中,没有排放到空气中,不会造成污染(答案合理即可)。

 Cu + H2O。
Cu + H2O。 
 H2O+Cu
H2O+Cu