某兴趣小组开展 “ 测定密闭容器中某种气体的体积分数 ” 的探究实验。
(实验 1 )按图 1 所示装置,用红磷燃烧的方法测定空气中氧气的体积分数。
(实验 2 )按图 2 所示装置,在集气瓶内壁用水均匀涂附铁粉除氧剂(其中辅助成分不干扰实验),利用铁锈蚀原理测定空气中氧气的体积分数。

( 1 )实验 1 中,红磷燃烧的主要现象是 _____ 。红磷熄灭后,集气瓶冷却至室温,打开 K ,水能倒吸入集气瓶的原因是 ________ 。
( 2 )为提高实验的准确性,以上两个实验都需要注意的事项是 ________ (写一点)。
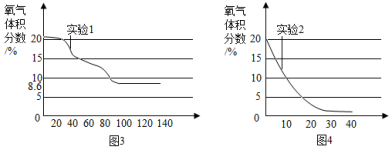
( 3 )实验过程中,连接数字传感器,测得实验 1 、实验 2 中氧气的体积分数随时间变化的关系分别如图 3 、图 4 所示。依据图 3 、图 4 信息, _____ (填 " 实验 1” 或 “ 实验 2" ) 的测定方法更准确,判断依据是 _____ 。
( 4 )结合你的学习经验,若要寻找红磷或铁粉除氧剂的替代物。用图 1 或图 2 装置测定空气中氧气的体积分数,该替代物应满足的条件是 _____ (写两点)。
(实验 3 )测定用排空气法收集到的集气瓶中二氧化碳的体积分数。
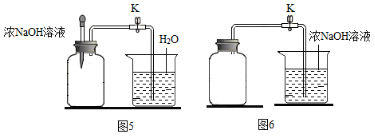
( 5 )甲同学设计图 5 所示装置进行测定。浓 NaOH 溶液的作用是 _____ (用化学方程式表示)。
( 6 )乙同学提出,仅利用图 6 所示装置,在不添加其他试剂的前提下,也能测得集气瓶中二氧化碳的体积分数。为达到实验目的,操作方法是 _____ 。
答案
产生大量白烟(或 “ 黄色火焰 ”“ 放热 ” 等合理答案) 氧气被消耗,集气瓶内气体压强小于大气压 装置的气密性良好(或 “ 红磷和铁粉除氧剂足量 ” 等其他合理答案) 实验 2 反应后,实验 1 集气瓶中剩余氧气的体积分数为 8.6% ,而实验 2 集气瓶中氧气几乎耗尽 能够和氧气反应,生成物不影响测定结果(或其他合理答案) 2NaOH + CO 2 =Na 2 CO 3 + H 2 O 用冰水冷却集气瓶,打开 K (或其他合理答案)
【分析】
红磷在氧气中点燃生成五氧化二磷,氢氧化钠和二氧化碳反应生成碳酸钠和水。
【详解】
( 1 )红磷在氧气中点燃生成五氧化二磷,实验 1 中,红磷燃烧的主要现象是产生大量白烟。红磷熄灭后,集气瓶冷却至室温,打开 K ,水能倒吸入集气瓶的原因是氧气被消耗,集气瓶内气体压强小于大气压。
( 2 )为提高实验的准确性,两个实验都需要注意的事项是装置的气密性良好。
( 3 )实验过程中,连接数字传感器,由实验 1 、实验 2 中氧气的体积分数随时间变化的关系可知,实验 1 集气瓶中剩余氧气的体积分数为 8.6% ,而实验 2 集气瓶中氧气几乎耗尽,故实验 2 的测定方法更准确,判断依据是反应后,实验 1 集气瓶中剩余氧气的体积分数为 8.6% ,而实验 2 集气瓶中氧气几乎耗尽。
( 4 )寻找红磷或铁粉除氧剂的替代物,用图 1 或图 2 装置测定空气中氧气的体积分数,替代物应满足的条件是能够和氧气反应 , 生成物不影响测定结果。
( 5 )氢氧化钠和二氧化碳反应生成碳酸钠和水,甲同学设计图 5 所示装置进行测定,故浓 NaOH 溶液的作用是吸收二氧化碳,化学方程式为 。
( 6 )只要存在压强差,则能产生倒吸,二氧化碳的体积分数,利用图 6 所示装置,在不添加其他试剂的前提下,操作方法是用冰水冷却集气瓶,打开 K 。
【点睛】
水能倒吸入集气瓶的原因是氧气被消耗,集气瓶内气体压强小于大气压。

 Cu + H2O。
Cu + H2O。 
 H2O+Cu
H2O+Cu