为探究碳还原氧化铜的最佳实验条件,用木炭粉和氧化铜的干燥混合物 1 ~ 2.5g 进行系列实验。
(查阅资料) ① 氧化铜( CuO )为黑色固体。
② 碳还原氧化铜得到的铜中可能含有少量的氧化亚铜;氧化亚铜为红色固体,能与稀硫酸反应: Cu 2 O+ H 2 SO 4 = CuSO 4 + H 2 O + Cu
(进行实验)
实验 1 :取质量比 1:11 的木炭粉和氧化铜混合物 1.3g ,进行实验。
| 序号 | 1-1 | 1-2 |
| 装置 | | |
| 反应后物质的颜色、状态 | 黑色粉末中混有少量红色固体 | 红色固体有金属光泽,混有极少量,黑色物质 |
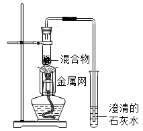
实验 2 :取一定量的混合物,用 1—2 装置进行实验。
| 序号 | 木炭粉与氧化铜的质量比 | 反应后物质的颜色、状态 | |
| 2-1 | 1:9 | 红色固体有金属光泽 | 混有少量黑色物质 |
| 2-2 | 1:10 | 混有很少量黑色物质 | |
| 2-3 | 1:11 | 混有极少量黑色物质 | |
| 2-4 | 1:12 | 无黑色物质 | |
| 2-5 | 1:13 | 混有较多黑色物质 | |
(解释与结论)
( 1 )配平化学方程式: ___C+___CuO 高温 ___Cu+ ___CO 2 ↑ 。
( 2 )实验 1—2 中,证明产生 CO 2 的现象是 _______________________ 。
( 3 )实验 1 的目的是 __________ 。
( 4 )实验 2 的结论是 _____________ 。
(反思与评价)
( 5 )实验 2 没有进行质量比为 1:14 的实验,理由是 ________________ 。
( 6 )为检验 2—4 的红色固体中是否含 Cu 2 O ,所需试剂是 __________ 。
答案
1 2 2 1 ; 澄清石灰水变浑浊; 探究木炭与氧化铜的受热面积对其反应的影响; 木炭与氧化铜质量比为 1:12 是恰好反应,因此木炭与氧化铜反应的最佳质量比为 1:12 ; 木炭与氧化铜质量比为 1:13 时,氧化铜已过量; 稀硫酸。
【详解】
( 1 )木炭与氧化铜反应方程式: C+2CuO 高温 2Cu+CO 2 ↑ ;
( 2 )二氧化碳使澄清石灰水变浑浊,故如看到澄清石灰水变浑浊,说明有二氧化碳生成;
( 3 )实验 1-1 ,反应物受热面积较大,实验 1-2 反应物受热面积较小,故实验 1 与实验 2 形成对比实验,可以探究木炭与氧化铜的受热面积对其反应的影响;
( 4 )由表可知,当木炭与氧化铜质量比为 1:12 是恰好反应,即木炭与氧化铜反应的最佳质量比为 1:12 ;
( 5 )由表可知,当木炭与氧化铜质量比为 1:13 时,氧化铜已过量,生成物中含有 Cu 和 CuO ,没有必要进行质量比为 1:14 的实验;
( 6 )因为 Cu 2 O + H 2 SO 4 = CuSO 4 + H 2 O + Cu ,所以向红色固体中加稀硫酸如溶液变为蓝色,可以可以说明有 Cu 2 O 。


 Cu + H2O。
Cu + H2O。 
 H2O+Cu
H2O+Cu