白云石粉是一种生产高级玻璃器皿、医药用瓶、光学玻璃的原料 ,某化学兴趣小组对白云石粉极其好奇,决定对其进行探究。
(查阅资料)
白云石属于碳酸盐矿物 ,白云石粉主要成分的化学式可表示为xMgCO 3 ·yCaCO 3 ( 杂质是二氧化硅,其不溶于水,也不与盐酸反应,受热不分解)
一、定性探究:白云石粉的成分和性质
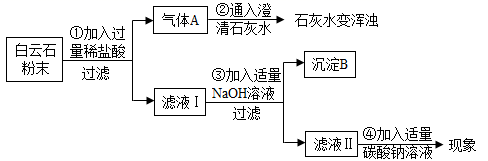
(实验分析)
(1)由步骤①②的现象可得出白云石粉中一定含有的离子是 _________ (填离子符号)。
(2)步骤③生成氢氧化镁的化学方程式是 ________ ;步骤 ④的反应现象是 _______ 。
(结论)综合上述实验现象可初步证明白云石由碳酸钙、碳酸镁组成。
(实验质疑)小组同学经过讨论认为 :因氢氧化钙微溶于水,导致沉淀B中除了氢氧化镁之外应该还混有氢氧化钙,对定量测定白云石粉的组成干扰较大,在老师的指导下该兴趣小组采用热分解法进行定量探究。
二、定量探究 :白云石的组成
(查阅资料)碳酸钙开始分解的温度为 898℃,1000℃时完全分解生成生石灰和二氧化碳气体;碳酸钙与碳酸镁的化学性质相似;碳酸镁开始分解的温度为540℃,700℃时完全分解。
(实验设计)为测定白云石中的含钙量及 x:y的值,该兴趣小组设计了如下装置并进行实验:
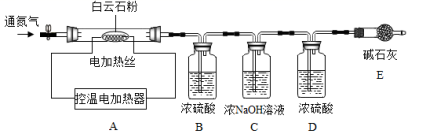
(实验步骤)
①组装仪器,检查装置的气密性;
②准确称取15.0g 白云石粉末放在A装置中,打开弹簧夹,鼓入一段时间氮气,称量B、C、D、E装置的质量;
③关闭弹簧夹,打开控温电加热器,缓缓调升温度至700℃,持续加热至固体质量不变;
④打开弹簧夹,缓缓鼓入一段时间氮气,准确称量B、C、D、E装置的质量;
⑤关闭弹簧夹,调升温度至1000℃,持续加热至固体质量不变,打开弹簧夹,缓缓鼓入一段时间氮气,准确称量B、C、D、E装置的质量。
实验数据记录如表 :
| | B中溶液质量/g | C中溶液质量/g | D中溶液质量/g | E的质量/g |
| 反应前 | 50.0 | 100.0 | 50.0 | 120.5 |
| 700℃ | 50.0 | 102.1 | 50.1 | 120.5 |
| 1000℃ | 50.0 | 106.3 | 50.3 | 120.5 |
(实验分析和数据处理)
(3)装置D的作用是 ______________________ 。
(4)持续加热至固体质量不变后缓缓鼓入一段时间氮气的目的是 __________ 。
(5)计算白云石中钙元素的质量分数 ______ 。 (写出计算过程,结果保留小数点后一位,)
(6)设计实验证明白云石粉已完全分解的实验方法是 ______ (写出实验方法、现象、结论)
(7)白云石(xMgCO 3 ·yCaCO 3 )中的 x:y= ________ (最简整数比),若加热前没有鼓入一段时间的氮气,将会导致 x:y的值 ___________ (填偏大、偏小或不变).
答案
![]()
![]() ═
═ ![]() ↓
↓ ![]() 产生白色沉淀 吸收氮气带出的水蒸气 ,防止测得二氧化碳的质量偏小 使残留在装置内的二氧化碳气体全部被 C装置吸收 26.7% 取少量反应后固体于试管中 ,加入足量的稀盐酸,无气泡产生,说明完全分解 1:2 偏大
产生白色沉淀 吸收氮气带出的水蒸气 ,防止测得二氧化碳的质量偏小 使残留在装置内的二氧化碳气体全部被 C装置吸收 26.7% 取少量反应后固体于试管中 ,加入足量的稀盐酸,无气泡产生,说明完全分解 1:2 偏大
【解析】
本题通过白云石粉研究,考查了实验探究物质的组成成分以及含量 , 过滤的原理、方法及其应用;常见气体的检验与除杂方法 , 盐的化学性质 , 书写化学方程式和根据化学反应方程式的计算 。 综合性较强,解题是时要充分利用 “查阅资料”弄清碳酸钙和碳酸镁的分解顺序,为数据处理提供依据。
( 1 )碳酸根离子能和氢离子结合成水和二氧化碳,因此由步骤 ①②的现象可得出白云石粉中一定含有的离子是 CO 3 2- ;
( 2 )步骤 ③中,氯化镁和氢氧化钠反应生成白色沉淀氢氧化镁和氯化钠,反应的化学方程式为: MgCl 2 +2NaOH═Mg(OH) 2 ↓+2NaCl; 氯化钙能和碳酸钠反应生成白色沉淀碳酸钙和氯化钠,实验现象是产生白色沉淀;
( 3) 气体从装置 C 出来的气体中含有少量的水蒸气。装置 D 的作用是吸收氮气带出的水蒸气,防止测得二氧化碳的质量偏小;
( 4) 持续加热至固体质量不变后缓缓鼓入一段时间氮气的目的是使残留在装置内的二氧化碳气体全部被 C 装置吸收;
( 5) 设碳酸钙的质量为 x,
碳酸钙分解生成二氧化碳质量 =(106.3g-102.1g)+( 50.3g-50.1g)=4.4g ,
CaCO 3 ![]() CaO+CO 2 ↑
CaO+CO 2 ↑
100 44
x 4.4g
x=10g ,
ω(Ca)═(10g×40%)/15g═26.7% ;
( 6) 若白云石粉已完全分解反应后固体中没有碳酸钙和碳酸镁,可用稀盐酸检验。实验证明白云石粉已完全分解的实验方法是:取少量反应后固体于试管中 , 加入足量的稀盐酸 , 无气泡产生 , 说明完全分解 ;
( 7 )设碳酸镁质量为 y ,
碳酸镁分解生成二氧化碳的质量 =(102.1g-100.0g)+(50.1g-50.0)=2.2g ,
MgCO 3 ![]() MgO+CO 2 ↑ ,
MgO+CO 2 ↑ ,
84 44
y 2.2g
y=4.2g ,
根据题意有: 84x:100y=4.2g:10g x:y=1:2 ;若加热前没有鼓入一段时间的氮气,导致测得的碳酸镁分解生成的二氧化碳质量偏大,从而会导致 x:y 的值偏大 。

 2MgO,其中各物质的质量之比为,m(Mg):m (O2):n(MgO)=48:32:80=3:2:5。
2MgO,其中各物质的质量之比为,m(Mg):m (O2):n(MgO)=48:32:80=3:2:5。 
 ×100%=
×100%= ×100%=1-杂质的质量分数
×100%=1-杂质的质量分数

 K2MnO4+MnO2+O2
K2MnO4+MnO2+O2 金属+水,该变化中固体质量减少量为生成水中氧元素的质量(或金属氧化物中氧元素的质量)
金属+水,该变化中固体质量减少量为生成水中氧元素的质量(或金属氧化物中氧元素的质量) 2H2O,反应后气体质量减小,其减小值为生成水的质量。
2H2O,反应后气体质量减小,其减小值为生成水的质量。 3Fe+4CO2
3Fe+4CO2

 ×2
×2 ×2=46
×2=46 ×2=24
×2=24 ×2=18
×2=18

 ):(70g×
):(70g× +30g×
+30g× )=35:352
)=35:352