硫酸亚锡( SnSO 4 )广泛应用于电镀工业。该物质易与氧气反应而变质。实验室模拟工业上制取 SnSO 4 的一种实验方案如下:
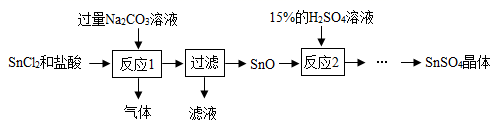
( 1)SnCl 2 由 Sn与盐酸反应制得,同时生成氢气,该反应的化学方程式为 _____ 。
( 2)Na 2 CO 3 俗称 _____ 。
( 3)过滤所得滤液中的溶质为 _____ (填化学式)。
( 4)用已知质量分数和密度的浓硫酸配制质量分数为15%的稀硫酸,所需玻璃仪器有烧杯、玻璃棒、胶头滴管和 _____ 。稀释浓硫酸的正确操作为 _____ 。
( 5)反应2属于基本反应类型中的 _____ 反应。从反应 2所得溶液中获得SnSO 4 晶体的部分操作须在隔绝空气条件下进行的原因是 _____ 。
答案
Sn+2HCl=SnCl 2 +H 2 ↑ 纯碱 SnCl 2 、 NaCl、Na 2 CO 3 量筒, 将浓硫酸沿烧杯壁慢慢注入水里,并用玻璃棒不断搅拌 复分解反应 防止 SnSO 4 晶体与氧气反应而变质
【分析】
活泼金属与稀盐酸或稀硫酸反应生成盐和氢气,根据流程图可以推测滤液中的溶质,根据溶液稀释的基本步骤可知所需的实验仪器有哪些,基本反应类型是分解反应、化合反应、置换反应和复分解反应。
【详解】
( 1 )锡和稀盐酸反应产生氯化亚锡和氢气,反应的化学方程式是 Sn+2HCl=SnCl 2 +H 2 ↑;(2)碳酸钠俗称是纯碱、苏打;(3)反应1有气体生成,是碳酸钠和盐酸反应生成氯化钠、水和二氧化碳,所以过滤之后的滤液中的溶质有氯化钠和氯化亚锡和过量的碳酸钠;(4)浓硫酸稀释的基本步骤为计算、量取、稀释,则需玻璃仪器有烧杯、玻璃棒、胶头滴管和量筒;稀释浓硫酸的正确操作是将浓硫酸沿烧杯壁慢慢注入水里,并用玻璃棒不断搅拌;(5)反应2是氧化亚锡和硫酸反应生成硫酸亚锡和水,是两种化合物互相交换成分生成另外两种化合物的反应,属于复分解反应;题干中硫酸亚锡易与氧气反应而变质,所以从反应2所得溶液中获得SnSO 4 晶体的部分操作须在隔绝空气条件下进行。

 CO2是碳充分燃烧的化学方程式。
CO2是碳充分燃烧的化学方程式。  2H2↑+O2↑为例加以说明。
2H2↑+O2↑为例加以说明。 