某同学设计的工业制备氢氧化钠的流程如下图。

资料 :
2NaCl+2H 2 O ![]() 2NaOH+H 2 ↑+Cl 2 ↑ ,两电极,一端得到 NaOH 和 H 2 ,另一端得到 Cl 2 。
2NaOH+H 2 ↑+Cl 2 ↑ ,两电极,一端得到 NaOH 和 H 2 ,另一端得到 Cl 2 。
(1) 晾晒海水得到粗盐的原理是 _______
(2) 实验室蒸发用到的仪器有铁架台 ( 带铁圈 )、 坩埚钳 、 石棉网、酒精灯、玻璃棒和 ________
(3) 工业生产中应选择途径 ______ (“ ① ” 或 “ ② ”), 理由是 ______
(4)Cl 2 可用于生产 84 消毒液 ( 有效成分 NaClO), 反应原理为 :Cl 2 +2NaOH=NaCl+NaClO+H 2 O ,反应前后氯元素的化合价有 ___ 种。
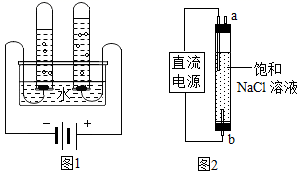
(5) 图 1 实验测定水的组成,不能加入 NaCl 增强水的导电性的理由是 ____ 。电解水的化学方程式为 ________
(6) 图 2 实验获得 84 消毒液,直流电源正极应与 ___ ( 填 a 或 b) 连接,才能使 NaClO 的含量更高。
答案
蒸发结晶 蒸发皿 ① 步骤简便,节约能源 3 加入 NaCl 后会有 Cl 2 的生成,干扰实验结果 2H 2 O ![]() 2H 2 ↑+O 2 ↑ b
2H 2 ↑+O 2 ↑ b
【解析】
(1) 晾晒海水得到粗盐是将海水引到盐池里进行蒸发,故原理是蒸发结晶;
( 2)实验室蒸发用到的仪器有铁架台 ( 带铁圈 )、 坩埚钳 、 石棉网、酒精灯、玻璃棒和蒸发皿;
( 3)工业生产中选步骤①,理由是步骤简便,节约能源 ;
( 4) 反应前氯气中氯元素的化合价为 0, 反应后,氯化钠中氯元素的化合价是 -1 价 , NaClO 中氯元素的化合价是 +1 价,故共有 3 种化合价 ;
( 5 )电解水实验中如加入氯化钠,会电解生成氯气,故不能加入氯化钠;水在通电的条件下反应生成氢气和氧气,反应方程式为: 2H 2 O ![]() 2H 2 ↑+O 2 ↑;
2H 2 ↑+O 2 ↑;
( 6 )电极 b 与氯化钠溶液接触更加充分,故接 b 极 ;

 100%=11.1%
100%=11.1%

 、
、

 、
、 
 、
、
 、
、
 、
、