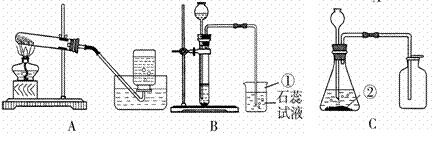
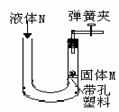
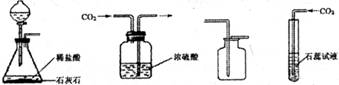
实验探究和证据推理是提升认知的重要手段。
(一)下图是某课外学习小组设计的气体制备与性质验证的组合实验,其中请看图回答下列问题:
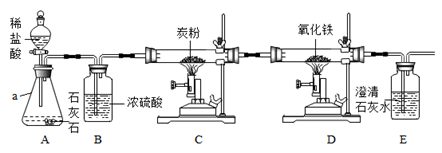
(1)仪器a名称为_____,A中发生反应的化学方程式_____;
(2)装置B的作用是干燥二氧化碳气体,利用了浓硫酸的_____;
(3)装置C中炭粉与干燥的二氧化碳反应产生一氧化碳。该反应中利用了炭粉的_____性;
(4)实验过程中装置D通入CO一段时间,待_____,再点燃酒精喷灯;
(5)反应一段时间后,观察到装置D玻璃管内粉末由_____色变成黑色,生成的黑色固体均能被磁铁吸引。
(6)该套装置中有一个明显的不足之处,你的改进方法是_____。
(二)化学兴趣小组对“CO还原Fe2O3粉末”的实验产生的黑色粉末继续进行探究:
(查阅资料)铁粉、FeO、Fe3O4均为黑色固体;铁粉、Fe3O4均能被磁铁吸引。
(提出猜想)对磁铁吸引的黑色固体成分有以下三种猜想:
猜测Ⅰ:Fe; 猜测Ⅱ:Fe3O4; 猜测Ⅲ:Fe和Fe3O4
(实验验证)取少量反应后的黑色固体放入试管中,加入足量的硫酸铜溶液,振荡,充分反应后静置,观察到红色固体中混有黑色颗粒,说明_____(填“猜想 Ⅰ”“猜想Ⅱ”或“猜想Ⅲ”)是正确的。
答案
锥形瓶 ![]() 吸水性 还原性 E中出现连续均匀的气泡时 红棕色 最后加一个燃着的酒精灯,或在导管口绑一个小气球 猜想Ⅲ
吸水性 还原性 E中出现连续均匀的气泡时 红棕色 最后加一个燃着的酒精灯,或在导管口绑一个小气球 猜想Ⅲ
【详解】
(一)(1)仪器a的名称是锥形瓶;
A中为石灰石中的碳酸钙与稀盐酸发生反应生成氯化钙、二氧化碳和水,该反应的化学方程式为:![]() ;
;
(2)装置B的作用是干燥二氧化碳气体,利用了浓硫酸的吸水性;
(3)装置C中炭粉与干燥的二氧化碳反应产生一氧化碳,在该反应中,炭粉得到氧,故该反应中利用了炭粉的还原性;
(4)因为一氧化碳具有可燃性,混有一定量的空气,遇明火会发生爆炸,故实验过程中,应先在装置D通入CO一段时间,将装置内空气排尽,待E中出现连续均匀的气泡时,再点燃酒精喷灯;
(5)一氧化碳能与氧化铁在高温的条件下反应生成铁和二氧化碳,氧化铁为红棕色,铁为黑色,故反应一段时间后,观察到装置D玻璃管内粉末由红棕色变成黑色;
(6)一氧化碳有毒,未反应的一氧化碳排到空气中,会污染空气,故应增加尾气处理装置,在最后加一个燃着的酒精灯,或在导管口绑一个小气球;
(二)实验验证:取少量反应后的黑色固体放入试管中,加入足量的硫酸铜溶液,振荡,充分反应后静置,铁能与硫酸铜反应生成硫酸亚铁和铜,四氧化三铁与硫酸铜不反应,反应后,观察到红色固体中混有黑色颗粒,说明猜想Ⅲ正确。