铁和铁的化合物在工农业生产中有广泛的应用。铁的冶炼和探究。取24.0g Fe2O3粉末,小组同学用如图装置模拟炼铁,并测定反应后固体成分。
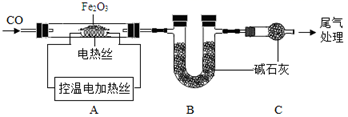
资料:碱石灰可吸收H2O和CO2。
(1)连接装置,先______________,再装入药品。
(2)实验时先通入CO,目的是_____________。
(3)①控制A中温度在700℃至固体全部变黑,继续通CO至冷却。目的是除了防止生成的Fe被氧化外还有_______________。
②通过测定装置B中固体的质量变化,可准确求得装置A中剩余固体质量。装置C的作用是_____________。
③现直接测得装置A中剩余固体质量为19.2g。则装置B中固体应增重_______g。
(4)经分析A中剩余固体19.2g为Fe和FexOy的混合物,向其中加入足量的稀H2SO4充分反应,得H2 0.3g。
①固体中Fe质量为________g。
②FexOy的化学式为________。
答案
检查装置的气密性 排尽装置的空气,防爆炸 把生成的CO2全部排出被B吸收 吸收空气中的二氧化碳和水蒸气 13.2 8.4 Fe5O4
【解析】
(1)有气体参加的反应,实验前需要检验装置的气密性,所以连接装置,先检查装置的气密性,再装入药品;
(2)CO具有可燃性,与玻璃管中的空气混合受热会发生爆炸,所以应先通CO排尽玻璃管中的空气,然后再加热;
(3)①控制A中温度在700℃至固体全部变黑,继续通CO至冷却。目的是除了防止生成的Fe被氧化外还有:把生成的CO2全部排出被B吸收;
②碱石灰能够吸收水和二氧化碳,所以装置C的作用是:吸收空气中的二氧化碳和水蒸气;
③测得装置 A 中剩余固体质量为19.2g,减少4.8g,就是氧元素的质量,所以
设生成二氧化碳质量为x
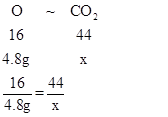
x=13.2g
所以装置B中固体应增重13.2g;
(4)设固体中铁的质量为y
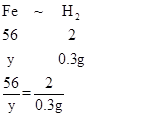
y=8.4g,
所以FexOy的质量为:19.2g-8.4g=10.8g
铁元素的质量为:10.8g-4.8g=6g,
铁、氧原子个数比为:![]()
所以FexOy 的化学式为Fe5O4。







