下图为实验室模拟炼铁,现将ag Fe2O3在高温下与足量CO反应,实验结束后测得B中产生6.00g白色沉淀,下列说法正确的是
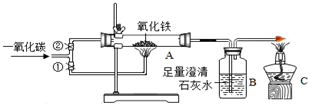
A.实验开始应该先打开弹簧夹① B.该实验过程中共消耗1.68 g CO
C.氧化铁质量为3.2g D.硬质玻璃管中固体由黑色变为红色
答案
C
【解析】
A、因为CO具有可燃性,混有氧气的CO点燃或加热可能发生爆炸,所以在该实验中,要先向放有氧化铁的玻璃管内通入CO,待玻璃管内空气排尽后方可加热,如果通CO和加热同时进行,可能发生爆炸,因此实验开始应该先关闭弹簧夹①,打开弹簧夹②,选项A不正确;
B、实验中发生了两个反应: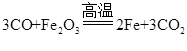 ,CO2+Ca(OH)2=CaCO3↓+H2O
,CO2+Ca(OH)2=CaCO3↓+H2O
题中已知生成碳酸钙沉淀6.00g,根据反应中的关系,CO和CO2是1∶1的关系,CO和CaCO 3也是1∶1的关系,设理论上需要一氧化碳质量为x,![]() 解得x=1.68g。但实际实验过程中要先通一氧化碳,反应后还要继续通一氧化碳至玻璃管冷却,反应中有部分一氧化碳没有参与反应,所以该实验中消耗的一氧化碳肯定超过1.68g。选项B不正确;
解得x=1.68g。但实际实验过程中要先通一氧化碳,反应后还要继续通一氧化碳至玻璃管冷却,反应中有部分一氧化碳没有参与反应,所以该实验中消耗的一氧化碳肯定超过1.68g。选项B不正确;
C、根据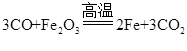 ,设Fe2O3的质量为y,
,设Fe2O3的质量为y,![]() ,解得y=3.2g,选项C正确;
,解得y=3.2g,选项C正确;
D、Fe2O3是红棕色粉末,铁粉是黑色粉末,所以实验中的现象应该是固体由红棕色变为黑色,选项D不正确。故选C。
【点睛】
一氧化碳还原氧化铁的实验中,反应开始要先通一氧化碳,后加热,反应结束还要继续通一氧化碳至玻璃管冷却,再加上反应中有部分一氧化碳没有参加反应,所以实际使用的一氧化碳量远超理论用量。







