据统计,我国每年报废的手机超过 1 亿部,若不进行有效回收利用,会造成巨大的浪费和污染。某种手机电路板中含有 Sn、Fe、Cu、Au、Ag 等金属。如图是某工厂回收其中部分金属的流程图。( 假设流程图中各反应均恰好完全反应。已知: 2Cu+O2+2H2SO4![]() 2CuSO4+2H2O)
2CuSO4+2H2O)
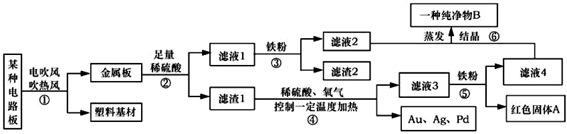
(1)步骤②中产生的气体是_______ ;步骤②~⑤都涉及到的操作是_______ ,其中用到的金属仪器是 ____ 。滤渣 1 中含有的金属是____ (选填字母)。
A Cu、Sn、Au、Pd B Cu、Au、Ag、Pd
C Sn、Au、Ag、Pd D Cu、Sn、Au、Ag
(2)已知 Sn 的化合价为+2 价,则步骤③反应的化学方程式为________ 。
(3)步骤⑥回收的纯净物 B 是________ (写名称)。
答案
H2 过滤 铁架台 B SnSO4+Fe=FeSO4+Sn 硫酸亚铁
【分析】
金属板加入足量的稀硫酸得到滤渣1和滤液1,滤渣1中加入稀硫酸、氧气控制温度加热,得到银、金和滤液3,滤液3中加入铁粉会生成红色固体A,所以A是铜,滤渣1中含有银、金、铜,滤液3是硫酸铜,滤液4是硫酸亚铁,所以铁、锡排在氢之前,滤液1中加铁得到硫酸亚铁和滤渣2,所以滤渣2中是锡。
【详解】
由分析可知:(1)步骤②中产生的气体是H2,步骤②~⑤都是将金属从溶液中分离出来,所以涉及到的操作是过滤,其中用到的金属仪器是铁架台,滤渣1中含有的金属是银、金、铜;
(2)步骤③的反应是硫酸锡和铁反应生成硫酸亚铁和锡,化学方程式为:SnSO4+Fe═FeSO4+Sn
(3)步骤⑥回收的纯净物B是硫酸亚铁。







