由氯化钡废液(杂质为FeCl3及微量NaCl)制备产品BaC12•2H2O的流程如图。
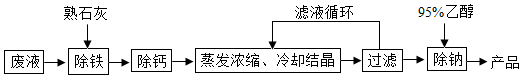
(1)氯化钡废液属于_____(填“纯净物”或“混合物”)。FeCl3中铁元素的化合价是_____。
(2)煅烧石灰石制取生石灰的化学方程式为_____,生石灰变成熟石灰的过程是_____过程(填“吸热”或“放热”),石灰水能使紫色石蕊试液变_____色。石灰石和熟石灰中常用于改良酸性土壤的是_____。
(3)用95%乙醇(C2H6O)洗涤滤渣可除微量NaCl.C2H6O由_____种元素组成,是_____化合物(填“有机”或“无机”)。C2H6O在O2中完全燃烧生成CO2和_____。2个CO2分子可用化学符号表示为_____。煤、氢气、乙醇三种燃料中,最清洁的是_____。
(4)结合流程和表回答:工业上选择25℃而不选择5℃进行冷却结晶的主要原因是①滤液多次循环后,25℃与5℃结晶产品的总产率基本相同;②_____。
表:每次结晶时,温度对产品纯度和产率的影响
| 冷却结晶的温度/℃ | 产品的纯度/% | 产品的产率/% |
| 5 | 99 | 72 |
| 25 | 99 | 60 |
答案
混合物 +3价 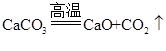 放热 蓝 熟石灰 3 有机 H2O 2CO2 氢气 25℃是常温,不需要专门降温
放热 蓝 熟石灰 3 有机 H2O 2CO2 氢气 25℃是常温,不需要专门降温
【解析】
(1)氯化钡废液中除了含有氯化钡、水外,还含有杂质FeCl3及微量NaCl,所以氯化钡废液属于混合物。FeCl3中氯元素显+1价,所以铁元素的化合价是:+3价。
(2)煅烧石灰石制取生石灰的化学方程式为: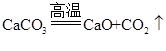 ;CaO+H2O=Ca(OH)2,反应中放热,所以生石灰变成熟石灰的过程是:放热过程;石灰水呈碱性,所以石灰水能使紫色石蕊试液变蓝色;石灰石难溶于水,而石灰水微溶于水且呈碱性,所以石灰石和熟石灰中常用于改良酸性土壤的是:熟石灰。
;CaO+H2O=Ca(OH)2,反应中放热,所以生石灰变成熟石灰的过程是:放热过程;石灰水呈碱性,所以石灰水能使紫色石蕊试液变蓝色;石灰石难溶于水,而石灰水微溶于水且呈碱性,所以石灰石和熟石灰中常用于改良酸性土壤的是:熟石灰。
(3)因为BaC12•2H2O易溶于水,不可用水洗涤,但用95%乙醇(C2H6O)洗涤滤渣可除微量NaCl,因为BaC12•2H2O难溶于酒精,95%乙醇又含有5%的水,能溶解微量氯化钠。从酒精的化学式C2H6O可知酒精由3种元素组成;它是含碳化合物,所以是:有机化合物;酒精中含氢,因此C2H6O在O2中完全燃烧除了生成CO2还有:H2O;因为化学式前面的数字表示分子的个数,所以2个二氧化碳分子可用化学符号表示为:2CO2;因为氢气燃烧后只生成水,而煤燃烧后有二氧化硫、一氧化碳等有害气体生成,乙醇燃烧如果不充分,也会生成一氧化碳等有害气体,所以煤、氢气、乙醇三种燃料中,最清洁的是:氢气。
(4)结合流程和表可知:工业上选择25℃而不选择5℃进行冷却结晶的主要原因是除了滤液多次循环后,25℃与5℃结晶产品的总产率基本相同外,因为25℃是常温,所以不需要专门降温,节约能源。因此第②个原因是:25℃是常温,不需要专门降温。
【点睛】
工业流程题解答问题要与实际生产相结合,比如降温结晶,理论上温度越低越好,但工业生产讲求效益,降温越低消耗的能量就越多,成本就越高。


