MgO在医药建筑等行业应用广泛。硫酸镁和木炭高温煅烧的产物为MgO(固体)、SO2、CO2、CO、硫蒸气。
(1)工业上,SO2的任意排放会引起的环境问题是_____。化石燃料燃烧是产生SO2的主要原因,下列做法能减少SO2排放的是_____ (填字母)。
a开发新能源替代化石燃料 b向高空排放SO2
(2)在高温、催化剂条件下,CO和H2可化合成燃料甲醇(CH3OH),该反应中CO和H2的分子个数比为_____。若CO和H2中混有H2S气体,H2S会与催化剂中的Cu在高温下发生置换反应,其中一种产物为CuS,该反应的化学方程式为_____。
(3)利用如图装置对硫酸镁和木炭进行高温煅烧,并对产生的四种气体进行分步吸收或收集。
已知:常温下,硫为固体;SO2、CO2均能与NaOH溶液反应。
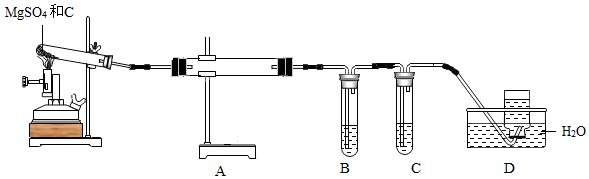
①装置B、C中的溶液分别是_____、_____。(填字母)
a NaOH溶液
b KMnO4溶液
②装置B、C的作用分别是_____、_____。
③装置D的作用是_____。
④若将装置A中的固体隔绝空气加热至500℃,就会变成蒸气,其中有一种相对分子质量为128的气体。该气体的化学式为_____。
答案
酸雨 a 1:2 Cu+H2S![]() CuS+H2 b a 吸收SO2 吸收CO2 收集CO S4
CuS+H2 b a 吸收SO2 吸收CO2 收集CO S4
【解析】
⑴ SO2的任意排放,在空气中经过一系列的变化生成硫酸,随雨水落下形成酸雨,所以SO2的任意排放会引起的环境问题是:酸雨;向高空排放SO2,只是稀释了空气中SO2并没有减少SO2的总量,开发新能源替代化石燃料可以减少SO2排放,所以能减少SO2排放的是:a。
⑵CO和H2在高温、催化剂条件下生成甲醇,化学方程式为: ![]() ,由化学方程式可知CO和H2的分子个数比为1:2;题中已知H2S和Cu在高温的条件下生成CuS和H2,所以化学方程式为:
,由化学方程式可知CO和H2的分子个数比为1:2;题中已知H2S和Cu在高温的条件下生成CuS和H2,所以化学方程式为:![]() 。
。
(3)因为硫酸镁和木炭高温煅烧的产物为MgO(固体)、SO2、CO2、CO、硫蒸气,气体混合物先通过A装置的长玻璃管,使硫蒸气冷却变成固体留到玻璃管内;因为SO2、CO2均能与NaOH溶液反应,CO2不与KMnO4溶液反应,CO既不与NaOH溶液反应,又不与KMnO4溶液反应,所以要先让SO2、CO2、CO通过装置B中的KMnO4溶液除去SO2,剩余气体继续通过C装置中的NaOH溶液除去CO2,因为CO难溶于水,再把CO通过D进行收集;所以:①装置B、C中的溶液分别是b、a;②装置B的作用是吸收SO2;装置C的作用吸收CO2;③装置D的作用是收集CO;
④设该气体的化学式为Sx
![]()
解得x=4,
该气体的化学式为:S4。
【点睛】
本题考查了镁、碳及其化合物、二氧化硫性质应用,以及化学方程式的书写,混合物分离方法和实验操作方法,对物质性质熟练掌握是解题关键。

 CO2是碳充分燃烧的化学方程式。
CO2是碳充分燃烧的化学方程式。  2H2↑+O2↑为例加以说明。
2H2↑+O2↑为例加以说明。 