为探究锌、铜、铬三种金属的性质,某兴趣小组进行如下实验。
(实验一)将三种金属丝分别与一节干电池和小电珠连接,小电珠发光。
(实验二)取粗细、长短相同的锌丝、铜丝、铬丝均与50mL稀硫酸反应,实验记录如下:
| 锌 | 铜 | 铬 | 铜 | |
| 稀硫酸的质量分数 | 5% | 5% | 15% | 15% |
| 反应现象 | 少量气泡 | 无现象 | 许多气泡 | 无现象 |
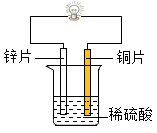
(实验三)金属锌、铜和稀硫酸构成如图所示的化学电池装置,观察到铜片表面有气泡(H2),小电珠发光。
(1)实验一的现象说明三种金属都具有____________性;
(2)铬与稀硫酸反应生成硫酸亚铬(CrSO4)和氢气,反应的化学方程式是______________________________________;该反应属于________________(填基本反应类型)反应;
(3)要判断三种金属活动性强弱,必须在实验二的基础上增补一个实验才能得出结论,其实验内容是把粗细、长短相同的________________放入________________的50mL稀硫酸中,观察放出气泡的快慢;
(4)金属活动性强弱是由金属物质的结构决定的,不会因某个实验而改变。下列关于实验三分析正确的是______(填序号)。
A.铜的金属活动性变得比锌强
B.铜与稀盐酸发生了置换反应
C.该装置将化学能转化为电能
答案
导电 Cr+H2SO4=CrSO4+H2↑ 置换 锌丝(或铬丝) 15%(或5%) C
【解析】
(1)实验一的现象说明三种金属都具有导电性;
(2)铬与稀硫酸反应的反应物是铬和硫酸,生成物是硫酸亚铬和氢气,氢气后面标上气体符号,所以方程式是:Cr+H2SO4=CrSO4+H2↑;
(3)由题目信息可知锌、铬的金属活动性都比铜强,接下来要判断锌和铬的活动性强弱,因此必须在实验二的基础上增补一个实验才能得出结论,其实验内容是:把粗细、长短相同的锌丝(或铬丝)放入15%(或 5%)的50mL稀硫酸中,观察放出气泡的快慢,放出气泡快并且多的金属活动性强;
(4)A、铜的金属活动性比锌弱,该选项说法不正确;
B、铜不能和稀盐酸反应,该选项说法不正确;
C、该装置将化学能转化为电能,该选项说法正确。故选C。
