根据如图所示的实验回答问题:
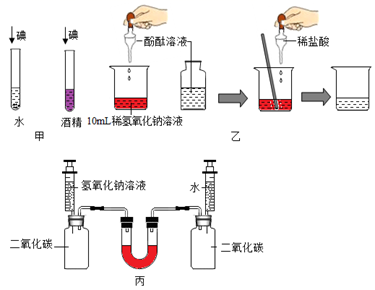
(1)实验甲探究的目的是_____。
(2)图乙实验的目的是_____,该反应的化学方程式是_____,该实验是通过检测_____来说明没有现象的化学反应一定发生的。
(3)图丙实验需要控制的变量是_____,观察到_____现象时说明二氧化碳与氢氧化钠发生反应,写出该反应的化学方程式_____。
答案
探究同一种物质在不同溶剂中的溶解能力是否相同 判断盐酸和氢氧化钠溶液能否发生化学反应 NaOH+HCl=NaCl+H2O 反应物消失(或减少) 加入的氢氧化钠溶液与加入的水的体积相同 U型管内左侧液面上升,右侧液面下降 ![]()
【详解】
(1)将碘分别放到等体积的水和酒精中可以比较碘在不同溶剂中的溶解性的大小,即探究同一种物质在不同溶剂中的溶解能力是否相同,故填探究同一种物质在不同溶剂中的溶解能力是否相同。
(2)将酚酞溶液滴加到氢氧化钠溶液中,溶液变为红色,再滴加稀盐酸并不断搅拌,观察到溶液逐渐变为无色,该实验通过指示剂的颜色变化来判断盐酸和氢氧化钠溶液能否发生化学反应,故填判断盐酸和氢氧化钠溶液能否发生化学反应;
盐酸与氢氧化钠发生中和反应生成氯化钠和水,故反应的化学方程式写为:NaOH+HCl=NaCl+H2O;
氢氧化钠溶液呈碱性,能够使酚酞溶液变红,随之盐酸的加入溶液的红色逐渐变淡,最后呈无色,说明氢氧化钠逐渐减少,最后不再存在,则该实验是通过检测反应物氢氧化钠的消失或减少来说明没有现象的化学反应一定发生的,故填反应物消失(或减少)。
(3)图丙中的实验目的是探究二氧化碳在氢氧化钠溶液和水中的溶解情况,根据控制变量法的要求,向两瓶二氧化碳中加入的氢氧化钠溶液与水的体积应该相同,故填加入的氢氧化钠溶液与加入的水的体积相同;
二氧化碳不仅溶于水,还能与氢氧化钠发生化学反应,所以实验过程中,左瓶中的二氧化碳减少得多,则观察到的现象是U型管内左侧液面上升,右侧液面下降,故填U型管内左侧液面上升,右侧液面下降;
二氧化碳与氢氧化钠反应生成碳酸钠和水,故反应的化学方程式写为:CO2+2NaOH=Na2CO3+H2O。

 CO2是碳充分燃烧的化学方程式。
CO2是碳充分燃烧的化学方程式。  2H2↑+O2↑为例加以说明。
2H2↑+O2↑为例加以说明。 