如图是甲、乙固体的溶解度曲线。下列说法正确的是( )
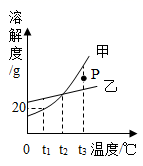
A.图中P点所表示的溶液是t3℃时甲的饱和溶液
B.可用t1℃时20%的甲溶液配制10%的甲溶液
C.若甲中含有少量乙,可采用冷却热饱和溶液的方法提纯甲
D.分别将t3℃等质量的甲、乙饱和溶液降温至t2℃,析出晶体质量相等
答案
C
【详解】
A、由图可知,图中P点在甲的溶解度曲线下方,即P点所表示的溶液是t3 ℃时甲的不饱和溶液,故A错误;
B、t1 ℃时,甲的溶解度为20g,溶液的最大浓度为其饱和溶液,其质量分数=![]() ×100%≈16.7%,不可能存在20%的溶液,故B错误;
×100%≈16.7%,不可能存在20%的溶液,故B错误;
C、甲、乙两物质的溶解度都随温度的升高而增大,甲的溶解度受温度的影响较大,乙物质的溶解度受温度的影响较小,故若甲中含有少量乙,可采用冷却热饱和溶液的方法提纯甲,故C正确;
D、由图可知,在t3 ℃时甲的溶解度大于乙,即等质量的甲、乙饱和溶液中甲溶液中溶剂的质量低于乙溶液中溶剂的质量,当降温至t2 ℃时,甲、乙溶解度相等,析出晶体的质量不相等,故D错误。故选C。