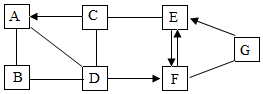
A~G都是初中化学常见的物质,它们的部分反应及转化关系如图所示。其中A为目前世界年产量最高的金属,A、B、C、D物质类别不同,其中C和D中不含相同的元素,E、F的组成元素相同。图中“→”表示转化关系,“﹣”表示相互反应关系(部分物质和反应条件未标出)。请完成下列问题:
(1)写出B的化学式_____;
(2)A和D反应的基本反应类型为_____;
(3)写出C﹣E反应的化学方程式_____;
(4)写出F→E反应的化学方程式_____,该反应伴随的能量变化是_____(填“放热”或“吸热”)。
答案
AgNO3 置换反应 3CO+Fe2O3![]() 2Fe+3CO2 2CO+O2
2Fe+3CO2 2CO+O2![]() 2CO2 放热
2CO2 放热
【解析】
A~G都是初中化学常见的物质,A为目前世界年产量最高的金属,所以A是铁,A、B、C、D物质类别不同,其中C和D中不含相同的元素,E、F的组成元素相同,C会转化成铁,氧化铁与一氧化碳在高温条件下反应生成铁和二氧化碳,所以C可以是氧化铁,D会与铁、氧化铁反应,所以D是盐酸,B会与盐酸、铁反应,所以B是硝酸银,盐酸会转化成F,E会与氧化铁反应,所以F是二氧化碳,E是一氧化碳,G会转化成一氧化碳,会与二氧化碳反应,所以G是碳,经过验证,推导正确。
【详解】
(1)由分析可知,B的化学式是AgNO3;
(2)A和D的反应是铁和盐酸反应生成氯化亚铁和氢气,基本反应类型为置换反应;
(3)C→E的反应是一氧化碳和氧化铁在高温的条件下生成铁和二氧化碳,化学方程式是:3CO+Fe2O3![]() 2Fe+3CO2;
2Fe+3CO2;
(4)F→E的反应是一氧化碳和氧气在点燃的条件下生成二氧化碳,化学方程式为:2CO+O2![]() 2CO2,该反应伴随的能量变化是放热。
2CO2,该反应伴随的能量变化是放热。
【点睛】
在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可。

 2Fe + 3CO2
2Fe + 3CO2 