工业上从海水中提取出含MgCl2、KCl两种物质的混合物,为了测定其中KCl的质量分数,现进行如下测定:取混合样品10.0g,向其中加入100g水,完全溶解后,分5次滴加KOH溶液,生成沉淀的质量与加入KOH溶液的质量关系如下表所示。
| 次数 | 第1次 | 第2次 | 第3次 | 第4次 | 第5次 |
| 滴加KOH溶液的质量/g | 10 | 10 | 10 | 10 | 10 |
| 产生沉淀的质量/g | 0.725 | 1.450 | 2.175 | 2.900 | 2.900 |
(1)通过表格可知,第 次滴加KOH溶液刚好完全反应。
(2)求反应后最终得到的混合溶液中KCl的质量分数。(计算结果精确到0.01%)
(3)请在坐标图中画出沉淀质量和加入KOH溶液质量的关系图。
(4)若用一定浓度的AgNO3溶液代替KOH,通过消耗硝酸银溶液质量来测定KCl的质量分数,测定值将会 (选填“偏大”“偏小”或“无影响”)。
答案
(1)4;(2)8.08%;(3);(4)偏大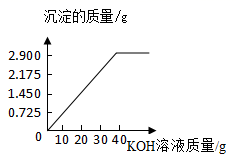
【详解】
(1)由表中的数据可知,每加入10g的氢氧化钾溶液产生沉淀的质量是0.725g,第四次加入时生成了沉淀是2.900g,再加入氢氧化钾不再生成沉淀,说明了第4次滴加KOH溶液刚好完全反应;
(2)设氯化镁的质量为x,生成的氯化钾的质量为y
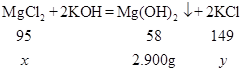
![]()
![]()
解得:x=4.750g y=7.45g
反应后最终得到的混合溶液中KCl的质量分数:![]() ≈8.08%
≈8.08%
答:反应后最终得到的混合溶液中KCl的质量分数为8.08%。
(3)由上述计算可知,加入40g的氢氧化钾溶液时恰好完全反应生成沉淀的质量为2.900g,作出图示如下:
(4)由于氯化镁、氯化钾都能与硝酸银反应生成氯化银沉淀,由消耗硝酸银溶液质量来测定KCl的质量分数,测定值将会偏大。


 B
B
 D
D