如图是 A、B、C 三种固体物质(均不含结晶水)的溶解度曲线,根据图示,下列说法正确的是
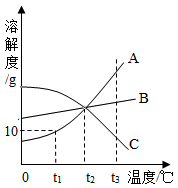
A.t1℃时,将A、B、C 各 10 g 放入50g水中,充分搅拌,所得溶液溶质质量分数均相等
B.t2℃时,A、B、C 溶液的质量分数一定相等
C.t3℃时,取相同质量的 A、B、C 三种饱和溶液降温到 t1℃,析出晶体最多的是 A,变成不饱和溶液的是 C
D.取 12gA 放入 t1℃时的 100g 水中,充分搅拌后全部溶解,说明 A 溶于水时吸热
答案
C
【详解】
A、t1℃时,将A、B、C 各 10 g 放入50g水中,充分搅拌,50g水中最多能溶解A的质量是5g,而B、C的溶解度都分别大于A的溶解度,所以50g水中溶解B、C的质量大于A的质量,则所得溶液溶质质量分数不相等,A不正确;
B、t2℃时,没有指明A、B、C溶液是否是饱和溶液,所以A、B、C 溶液的质量分数不一定相等,B不正确;
C、t3℃时,取相同质量的 A、B、C 三种饱和溶液降温到 t1℃,已知A、B的溶解度都随温度的升高而增大,但A的溶解度随温度变化比B的大,所以降温时A析出晶体较多,而C的溶解度随温度升高而减小,降温没有晶体析出,反而变成不饱和溶液,C正确;
D、t1℃时,100g水中最多能溶解10gA,现取12gA 放入 t1℃时的100g水中,充分搅拌后全部溶解,说明 A 溶于水时放热,使溶液的温度升高,A的溶解度增大,D不正确。故选C。



