(2018·盐城)盐城盛产海盐。某化学兴趣小组同学在市场购到粗盐,带回实验室进行提纯。
(1)在溶解、过滤、蒸发等操作中,均用到的玻璃仪器是 (填仪器名称)。
(2)配制50 g质量分数为6%的NaCl溶液,需称量NaCl固体 g,若用粗盐配制上述溶液,则所配溶液中NaCl的质量分数会 (填“偏大”“偏小”或“无影响“)。
探究活动:以NaCl为原料可以制取金属钠。兴趣小组同学认为Na是活泼金属,能与CuSO4等盐溶液反应,生成相应的金属单质。
(提出问题)Na与CuSO4溶液反应,是否有Cu生成?
(设计实验)兴趣小组同学在老师的指导下,设计了图所示装置进行实验。
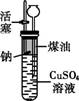
Ⅰ.向大试管中加入一定体积煤油。
Ⅱ.用小刀切一小块钠,放入大试管,塞上橡皮塞。
Ⅲ.打开活塞,通过长颈漏斗向试管中加入CuSO4溶液,使煤油的液面升至胶塞,关闭活塞,观察现象。
(实验现象)
(1)Na在煤油与溶液交界处上下来回振动,表面产生气泡,逐渐变小直至消失。
(2)溶液颜色逐渐变淡,有蓝色絮状沉淀和少量黑色固体生成。
(3)打开活塞,用燃着的木条放在尖嘴管口处,气体被点燃。
(查阅资料)①Na通常存放在煤油中;
②煤油不溶于水且不与水反应;
③2Na+2H2O![]() 2NaOH+H2↑;
2NaOH+H2↑;
④Cu(OH)2![]() CuO+H2O。
CuO+H2O。
(实验分析)
(1)根据上述信息,可获知金属钠的物理性质是 (答出一点即可)。
(2)实验中长颈漏斗的作用 (填序号)。
①便于添加CuSO4溶液
②收集气体
③防止压强过大冲开活塞
(3)对于产生的气体,有些同学猜想是H2,有些同学猜想是SO2。小组同学经过讨论,排除了SO2,理由是 。经过进一步实验,确认气体是H2。
(4)将反应后的混合物过滤,向滤渣中滴加足量稀硫酸,滤渣完全溶解。写出滤渣与稀硫酸反应的化学方程式 (写出一个即可)。
(实验结论)Na与CuSO4溶液反应,无Cu生成。
(实验反思)Na与CuSO4溶液反应无Cu生成,原因可能是 。
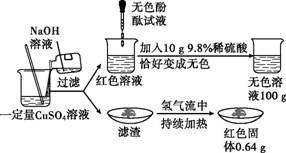
(定量分析)另取一定量上述CuSO4溶液,完成下列实验。利用数据计算无色溶液的溶质质量分数。(写出计算过程,滴入的酚酞试液质量忽略不计)
答案
(1)玻璃棒 (2)3 偏小
(实验分析)(1)硬度小(或密度比水小,比煤油大)
(2)①③
(3)SO2不可燃
(4)Cu(OH)2+H2SO4![]() CuSO4+2H2O(或CuO+H2SO4
CuSO4+2H2O(或CuO+H2SO4![]() CuSO4+H2O)
CuSO4+H2O)
(实验反思)钠的化学性质非常活泼,会先与硫酸铜溶液中的水反应生成NaOH
(定量分析)解:分析知此无色溶液为硫酸钠溶液,生成红色固体Cu的质量为0.64 g根据质量守恒定律可知滤渣Cu(OH)2的质量为0.98 g。
设与CuSO4反应生成硫酸钠的质量为x。
2NaOH+CuSO4![]() Cu(OH)2↓+Na2SO4
Cu(OH)2↓+Na2SO4
98 142
0.98 g x
![]()
x=1.42 g
设与H2SO4反应产生的硫酸钠的质量为y。
H2SO4+2NaOH![]() Na2SO4+2H2O
Na2SO4+2H2O
98 142
10 g×9.8% y
![]()
y=1.42 g
所以无色溶液的溶质质量分数为![]() ×100%=2.84%。
×100%=2.84%。
答:无色溶液的溶质质量分数为2.84%。