下列是初中化学中的一些重要实验(图1),请回答:
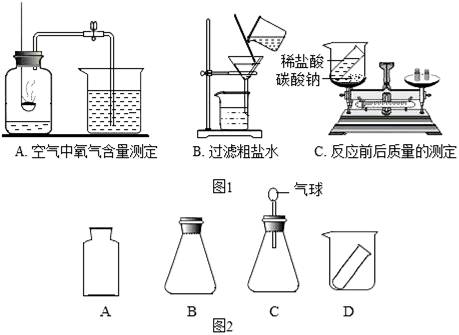

(1)A中红磷必须足量的原因是 ;
(2)B中玻璃棒的作用是 ;
(3)C中反应后天平不平衡,该反应是否遵守质量守恒定律 (填“是”或“否”);
(4)小明同学换用石灰石和稀盐酸反应来验证质量守恒定律,最合理的实验装置是(图2) (填序号)
答案
【考点】质量守恒定律及其应用;过滤的原理、方法及其应用;空气组成的测定.
【专题】化学用语和质量守恒定律;空气与水.
【分析】(1)根据实验的原理及注意的事项分析红磷过量原因.
(2)根据玻璃棒在过滤操作的作用来分析;
(3)根据质量守恒定律的适用范围来分析;
(4)有气体或烟生成的反应在验证质量守恒定律时应在密闭装置中进行.
【解答】解:(1)该实验主要是利用物质燃烧消耗装置内的氧气,然后根据进入水的体积,判断氧气的体积.只有加入过量的红磷,才能将将氧气完全消耗掉.如果红磷的量不足,会导致实验的结果是水倒流不足五分之一;
(2)在过滤操作中,玻璃棒的作用是引流;
(3)所有的化学变化都遵循质量守恒定律;
(4)有气体或烟生成的反应在验证质量守恒定律时应在密闭装置中进行,为防止气压增大,瓶塞冲出,最好采用C装置.
故答案为:(1)为了耗尽装置内的氧气;
(2)引流;
(3)是.
(4)C.
【点评】此题以图示的形式综合考查了正确判断实验现象及规范进行基本的实验操作的综合题,解题时应充分利用题中给予的信息,进行筛选分析,得出正确答案.



 五氧化二磷
五氧化二磷