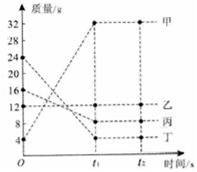
将一定质量的甲、乙、丙、丁四种物质放入密闭容器中,在一定条件下发生反应.反应前及t1、t2时各物质质量如图所示.关于该实验,下列说法中错误的是( )

A.反应后容器中甲物质的质量为32g
B.参加反应的丙与生成的甲的质量之比为1:4
C.参加反应的丙、丁的质量之比为2:5
D.乙可能是该反应的催化剂
答案
【考点】质量守恒定律及其应用;催化剂的特点与催化作用.
【专题】化学用语和质量守恒定律.
【分析】根据质量守恒定律,在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和.
反应后质量增加的是生成物,减少的是反应物,由图中信息可知:反应后甲质量增加了32g﹣4g=28克,是生成物;丁质量减少了24g﹣4g=20克,是反应物;乙质量不变,可能做催化剂;反应物应该还少8克,所以丙是反应物,故反应物是丙和丁,生成物是甲,是化合反应.
【解答】解:A、反应后容器中甲物质的质量为32g,正确;
B、参加反应的丙与生成的甲的质量之比为:(24g﹣8g):(32g﹣4g)=4:7,错误;
C、参加反应的丙、丁的质量之比为:8:20=2:5,正确;
D、乙质量不变,可能做催化剂;正确.
故选B.
【点评】本题是运用化学中的基本思想质量守恒思想,通过归纳不同物质或不同变化过程中相同点和不同点有效地寻找出它们之间的内在联系以及融合点和嫁接点,从而培养了学生的创新思维能力.



 五氧化二磷
五氧化二磷