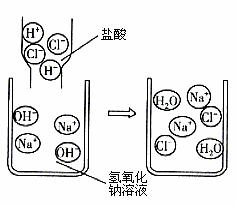
实验室有一瓶标签被腐蚀的无色溶液,是稀硫酸和氢氧化钠溶液中的一种。在老师的指导下,小红和小明用不同方法鉴定。
实验一:
| 实验步骤 | 实验现象 | 实验结论 |
| 小红取少量该溶液于试管中,向其中插入没有打磨的铝片 | 开始无明显现象,后产生______ | 小红认为该溶液为稀硫酸 |
| 小明用pH试纸测定其pH | pH=13 | 小明认为该溶液为氢氧化钠溶液 |
小红和小明操作均无误。
【提出问题】
该溶液到底是稀硫酸还是氢氧化钠溶液?
【查阅资料】
铝、氧化铝既能与酸反应,又可与强碱溶液反应,2Al+2NaOH+2H2O=2NaAlO2+3H2↑,氧化铝与氢氧化钠溶液反应生成偏铝酸钠( NaAlO2)和一种氧化物。NaAlO2易溶于水,其水溶液呈碱性,NaAlO2与铝、氧化铝均不反应。
【分析实验得出结论】该溶液为______溶液。
【交流反思】实验一中,小红所做实验开始无明显现象的原因是______。(用化学方程式表示)
【拓展应用】有一种管道疏通剂,主要成分为铝粉和氢氧化钠粉末。工作原理是:利用铝和氢氧化钠遇水反应放出大量的热,加快氢氧化钠对油脂和毛发等淤积物的腐蚀,同时产生氢气增加管道内气压,利于疏通。
实验二:小明用如图所示的玻璃弯管模拟家庭下水道,并用动物脂肪和毛发堵在弯管处,他按照使用说明从左端管口加入管道疏通剂,并用胶塞堵住弯管左端上口,
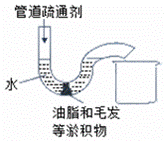
可能出现的现象为______(填字母序号)。
A.产生大量气体
B.弯管内温度升高
C.堵塞物变软被气体赶出,落入烧杯中
实验三:为了证明烧杯中废液里是否还含有氢氧化钠,小明做了如下实验
| 实验操作 | 实验现象 | 实验结论 |
| 取少量澄清废液于试管中,滴入酚酞 | 溶液变红 | 废液中有氢氧化钠剩余 |
小红对小明的结论提出了质疑,理由是______,小红把酚酞改用______(填药品)进行实验,得出废液中还含有氢氧化钠。
管道疏通剂中氢氧化钠过量,可确保铝粉反应完全,并且过量的氢氧化钠对下水道有清污的作用。
答案
气泡,铝片逐渐溶解 氢氧化钠 Al2O3+2NaOH+=2NaAlO2+H2O ABC NaAlO2易溶于水,其水溶液呈碱性,也能使无色酚酞试液变红 硫酸铜溶液
【解析】
解:实验一:小红认为该溶液为稀硫酸,是因为她看到的现象是:气泡,铝片逐渐溶解;
【分析实验得出结论】因为溶液的pH=13,溶液呈碱性,是氢氧化钠溶液;
【交流反思】铝表面有一层致密的氧化铝保护膜和氢氧化钠溶液反应生成偏铝酸钠和水,化学方程式为:Al2O3+2NaOH+=2NaAlO2+H2O;
实验二:根据“工作原理是:利用铝和氢氧化钠遇水反应放出大量的热,加快氢氧化钠对油脂和毛发等淤积物的腐蚀,同时产生氢气增加管道内气压,利于疏通。
”可知,ABC是正确的;
实验三:NaAlO2易溶于水,其水溶液呈碱性,也能使无色酚酞试液变红。取少量澄清废液于试管中,滴入酚酞,溶液变红色,并不能说明废液中一定有有氢氧化钠剩余;小红把酚酞改用硫酸铜溶液,如果溶液变浑浊,有蓝色沉淀生成,说明废液中还含有氢氧化钠。
故答案为:
实验一:气泡,铝片逐渐溶解;
【分析实验得出结论】氢氧化钠;
【交流反思】Al2O3+2NaOH+=2NaAlO2+H2O;
实验二:ABC;
实验三:NaAlO2易溶于水,其水溶液呈碱性,也能使无色酚酞试液变红;硫酸铜溶液。
实验一:根据铝和稀硫酸反应生成氢气进行分析;

 Na2CO3+H2O+CO2↑;然后2NH4Cl+Ca(OH)2==2NH3↑+CaCl2+H2O
Na2CO3+H2O+CO2↑;然后2NH4Cl+Ca(OH)2==2NH3↑+CaCl2+H2O  Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑  Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑