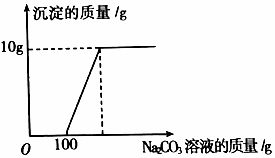
小明同学在完成实验室制取CO2后,对回收的盐酸和CaCl2混合溶液(不考虑其它杂质)进行以下实验:取200g该溶液于烧杯中,向其中滴加溶质质量分数为10.6%的Na2CO3溶液,滴入Na2CO3溶液与生成沉淀的质量关系如图所示。
(1)生成沉淀的质量为 g?
(2)回收液中HCl的质量分数是多少?
(3)当Na2CO3溶液与CaCl2溶液恰好完全反应时,溶液中溶质的质量是多少?
答案
解:(1)由图象可知,生成沉淀的质量为10g;
(2)由图中数据可知与HCl反应的碳酸钠溶液的质量为:100g×10.6%=106g。
设回收液中HCl的质量分数是x、生成氯化钠的质量为y,
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 73 117
10.6g 200g×x y
解得:x=3.65g y=11.7g
(2)设碳酸钠与氯化钙反应生成的氯化钠的质量为m。
Na2CO3+CaCl2=CaCO3↓+2NaCl
100 117
10g m
解得:m=11.7g
当Na2CO3溶液与CaCl2溶液恰好完全反应时,溶液中溶质的质量:11.7g+11.7g=23.4g。
答案:(1)10;
(2)回收液中HCl的质量分数是3.65%;
(3)溶液中溶质的质量是23.4g。
