某品牌饮用水中含有较多的碳酸氢钙[Ca(HCO3)2],属于硬水,煮沸时会有水垢生成,实验小组欲探究该水垢的主要成分。
【猜想与分析】分析Ca(HCO3)2与水的元素组成,该水垢的主要成分可能是___。
Ⅰ:CaO Ⅱ:Ca(OH)2
Ⅲ:CaCO3 Ⅳ:Ca(OH)2和CaCO3
小强同学认为该水垢中不会存在CaO,理由是__。
【实验与事实】
| 实验 | 现象 | 解释或结论 | |
| 实 | |||
| 验 | |||
| 一 | 将适量的水垢和水装入试管中,充分振荡后静置,用滴管取上层清液于小试管中,然后再向小试管中滴入紫色石蕊溶液 | 紫色石蕊溶液不变色 | Ca(OH)2微溶于水,其水溶液显碱性,能使紫色石蕊溶液变蓝色,不变色说明水垢中一定没有___ |
| 实 | |||
| 验 | |||
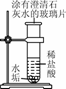
| 二 | 按如图所示方案进行实验 | ||
|
| 反应一段时间后水垢消失,溶液澄清;玻璃片上澄清石灰水变浑浊 | 石灰水变浑浊,说明有CO2生成,则水垢中一定含有__ |
【原理与呈现】请用化学方程式表示实验二中有关反应的化学反应原理:__ __,__ __。
【实践与应用】使用硬水会给生活和生产带来许多麻烦,长期饮用硬水对人体健康不利,在日常生活中,可使用__ __来检测饮用水是硬水还是软水。
答案
Ⅲ_ CaO能与水反应___Ca(OH)2 CaCO3
CaCO3+2HCl===CaCl2+H2O+CO2↑CO2+Ca(OH)2===CaCO3↓+
H2O肥皂水