在20℃时,配制100g溶质质量分数为5%的氯化钠溶液,以下是实验操作示意图,请回答下列问题.
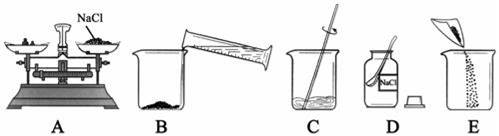

(1)上述实验操作中有一处明显的错误,请指出: (填序号).C中玻璃棒的作用是 .
(2)配制上述溶液需要氯化钠的质量为 g,应该选择 (填“10”、“50”或“100”)ml的量筒量取所需的水.
(3)操作步骤可概括为:计算、 、量取、溶解、装瓶贴标签等.
(4)误差分析:在量取水的体积时如果俯视读数,则导致所配溶液的溶质质量分数 (填“偏大”、“偏小”或“不变”).
(5)若将100g 5%的氯化钠溶液质量分数增大一倍,应蒸发 克水.
答案
【考点】一定溶质质量分数的溶液的配制.
【专题】化学学习中的实验思想;溶液、浊液与溶解度.
【分析】(1)根据托盘天平的使用要遵循“左物右码”的原则,C是溶解操作,进行分析解答.
(2)利用溶质质量=溶液质量×溶质的质量分数,可根据溶液的质量和溶质的质量分数计算配制溶液所需要的溶质的质量;再根据溶剂质量=溶液质量﹣溶质质量即可求得水的质量,进而确定所需量筒的量程.
(3)根据配制溶质质量分数一定的溶液的步骤,进行分析解答.
(4)在量取水的体积时如果俯视读数,读数比实际液体体积大,进行分析解答.
(5)根据溶液蒸发前后溶质的质量不变,进行分析解答.
【解答】解:(1)托盘天平的使用要遵循“左物右码”的原则,图A中所示操作砝码与药品位置放反了.
C是溶解操作,玻璃棒的作用是搅拌,加快溶解速率.
(2)溶质质量=溶液质量×溶质的质量分数,配制100g溶质质量分数为5%的氯化钠溶液,需氯化钠的质量=100g×5%=5g;溶剂质量=溶液质量﹣溶质质量,则所需水的质量=100g﹣5g=95g(合95mL);应用规格为100mL的量筒量取水的体积.
(3)配制100g溶质质量分数为5%的氯化钠溶液,首先计算配制溶液所需氯化钠和水的质量,再称量所需的氯化钠和量取水,最后进行溶解.
(4)在量取水的体积时如果俯视读数,读数比实际液体体积大,会造成实际量取的水的体积偏小,则使溶质质量分数偏大.
(5)设要蒸发水的质量为x,根据溶液蒸发前后溶质的质量不变,
则100g×5%=(100g﹣x)×10% x=50g.
故答案为:(1)A;搅拌,加快溶解速率;(2)5;100;(3)称量;(4)偏大;(5)50.
【点评】本题难度不大,掌握配制溶质质量分数一定的溶液的步骤(计算、称量、溶解)、溶质质量=溶液质量×溶质的质量分数、溶剂质量=溶液质量﹣溶质质量等是正确解答本题的关键.



