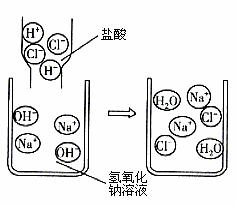
老师请小刚帮助他将失去标签的盐酸、氯化钠、氢氧化钠三瓶溶液鉴别出来,并重新贴好标签.为了鉴别这三种溶液,小刚取这三种溶液各少许,分别编号为A、B、C,按如图步骤进行实验,同时观察现象.
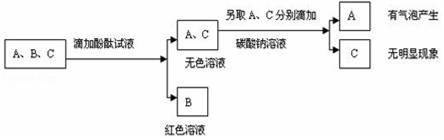

由此推断出:A为 溶液,B为 溶液,C为 溶液.检验产生的气体为二氧化碳的化学方程式是 .
答案
【考点】酸、碱、盐的鉴别;书写化学方程式.
【专题】物质的鉴别题;物质的检验、鉴别与推断.
【分析】盐酸、氯化钠、氢氧化钠三瓶溶液分别显酸性、中性、碱性,结合无色酚酞溶液遇酸性溶液不变色,遇碱性溶液变红,碳酸钠能与酸反应生成气体,进行分析解答.
【解答】解:盐酸、氯化钠、氢氧化钠三瓶溶液分别显酸性、中性、碱性,小刚取这三种溶液各少许,分别滴加无色酚酞溶液,分别显示无色、无色、红色,故A、C为盐酸、氯化钠中的一种,B为氢氧化钠溶液;另取A、C滴加碳酸钠溶液,碳酸钠与稀盐酸反应生成二氧化碳气体,与氯化钠溶液不反应,故A为稀盐酸,C为氯化钠溶液.
检验产生的气体为二氧化碳,应用澄清的石灰水,二氧化碳与氢氧化钙反应生成碳酸钙沉淀和水,反应的化学方程式为:CO2+Ca(OH)2=CaCO3↓+H2O.
故答案为:盐酸;氢氧化钠;氯化钠;CO2+Ca(OH)2=CaCO3↓+H2O.
【点评】本题有一定难度,解答物质的鉴别题时要熟练掌握鉴别的物质的性质,然后选择适当的试剂或方法,出现不同的现象即可鉴别.

 Na2CO3+H2O+CO2↑;然后2NH4Cl+Ca(OH)2==2NH3↑+CaCl2+H2O
Na2CO3+H2O+CO2↑;然后2NH4Cl+Ca(OH)2==2NH3↑+CaCl2+H2O  Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑  Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑