结合下列与铁有关的实验,回答问题:

(1)A实验中,按照图示实验,容易导致的不良后果是___________;
(2)B实验中,有关反应可用化学方程式表示为___________;
(3)C实验中,在硫酸铜溶液中的铁丝表而能够观察到的明显现象是___________;
(4)D实验中,a与c对比,说明铁生锈的条件之一是___________。
(1)集气瓶底炸裂 (2)![]() (3)有红色固体析出 (4)与氧气接触
(3)有红色固体析出 (4)与氧气接触
【解析】(1)细铁丝在纯氧气中燃烧时,为了防止铁的熔化物温度过高而炸裂集气瓶,应该在瓶底放少量水或细沙,按照图示实验,容易导致的不良后果是集气瓶底炸裂;(2)铁与盐酸反应生成氯化亚铁和氢气,化学方程式为:Fe+2HCl=FeCl2+H2↑;(3)铁与硫酸铜反应生成硫酸亚铁和铜,实验现象为:铁丝表面有红色固体析出,溶液由蓝色变浅绿色;(4)D实验中,a与c对比,反应条件的差别是是否与氧气接触,说明铁生锈的条件之一是与氧气接触。
某校同学开展了如下“溶液酸碱性的检验”的实验活动:

(1)把自制的紫色紫薯汁按图1所示分别滴加到试管中,观察到的现象如下表所示:
| 溶液 | 白醋 | 盐酸 | 食盐水 | 草木灰水 | 石灰水 |
| 加入紫薯汁后的颜色 | 红色 | 红色 | 紫色 | 绿色 | 绿色 |
①图1中存放紫薯汁的仪器名称_____;
②据上表推测,紫薯汁能做酸碱指示剂,遇到稀硫酸溶液可能显示的颜色是_____,该汁液______(填“能”或“不能”)做酸碱指示剂。
(2)用pH试纸测定图1中部分溶液的酸碱度:草木灰水pH>7,属于_____(填“酸性”、“中性”或“碱性”)溶液,白醋pH_____(填“>”、”<”或”=”)7。
(3)图2是三位同学分别测定土壤酸碱度的操作示意图,其中正确的是_____(填“A”、“B”或“C”,下同),可能导致所测溶液pH数值发生改变的错误操作是_____。
(1)①滴瓶; ②红色; 能;
(2)碱性; <;
(3)B; C。
【解析】(1)①根据实验室常用仪器可知:存放紫薯汁的仪器名称是滴瓶;②上表推测,紫薯汁遇到稀硫酸溶液可能显示的颜色是红色,紫薯汁在酸碱溶液中显示不同颜色,可以作为酸碱指示剂;(2)用pH试纸测定图1中部分溶液的酸碱度:草木灰水pH>7,属于碱性溶液;白醋pH<7;(3)正确的pH试纸的使用方法是取待测液少许,滴在pH试纸进行检验,故答案为B;把pH试纸润湿会使溶液被稀释导致数值不准确,A直接放入待测液中会使溶液被污染,故答案为C。
某化学兴趣小组三位同学在学习盐酸与氢氧化钠反应后,结合自己在实验室中所做的实验,分别从不同方面对其进行图画描述。图A是实际操作图,图B是反应过程中溶液的酸碱度变化图,图C是微观粒子结合过程的示意图。根据图示回答下列问题:
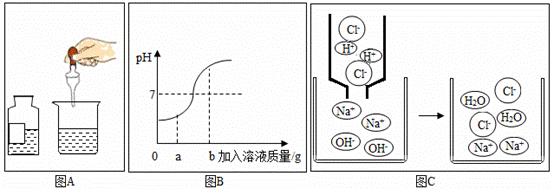
(1)该变化对应的实验操作是将______溶液滴加到另一种溶液中;
(2)当滴入溶液的质量为ag时,溶液中的溶质为_____、_____(填化学式);
(3)当溶液的![]() 时,溶液中的主要离子是______、______(填离子符号);
时,溶液中的主要离子是______、______(填离子符号);
(4)当加入溶液的质量为bg时,向所得溶液中滴加紫色石蕊试液,溶液是______色。
(1)盐酸
(2) NaCl NaOH
(3) Na+ Cl-
(4) 红
【解析】(1)坐标的pH变化是由大于7到小于7的过渡,因此进行的操作是将盐酸溶液滴加到氢氧化钠中。(2)当加入溶液的质量为ag时,溶液呈现碱性,所得溶液中的溶质为氯化氢和氢氧化钠。(3)当溶液的pH=7时,酸碱恰好完全反应,溶液中的主要离子是(些离子符号)钠离子和氯离子;(4)当加入溶液的质量为bg时,所得溶液显酸性,能使石蕊试液变红色。
实验小组的同学研究氢氧化钠、氢氧化钙两种物质的化学性质时,进行了如下所示的实验,并归纳出碱的通性(如图所示,连线表示相互反应)。

(1)图2中实验后某试管中的液体呈红色,则试管中原来盛有的物质是_____;
(2)图1中实验后某试管的底部有蓝色沉淀,写出反应的化学方程式_____,该反应属于_____(填基本反应类型);
(3)性质决定物质的用途,能用铁器盛放氢氧化钠固体,原因是_____;
(4)写出上述发生中和反应的化学方程式_____(写出1个即可);
(5)归纳通性的图中A所表示的物质类别是_____;
(6)不同碱具有相似性质,但性质也存在差异。氢氧化钙溶液能与碳酸钠溶液反应,而氢氧化钠则不能,其原因是_____。
(1)无色酚酞试液
(2)2NaOH+CuCl2═Cu(OH)2↓+2NaCl 复分解反应
(3)氢氧化钠不与铁反应
(4)NaOH+HCl═NaCl+H2O或Ca(OH)2+2HCl═CaCl2+2H2O
(5)非金属氧化物
(6)氢氧化钠和氢氧化钙溶于水解离出的阳离子不同,或氢氧化钠溶液中有钠离子,而氢氧化钙溶液中存在的是钙离子
【解析】(1)澄清石灰水显碱性,能使酚酞试液变红色;(2)氢氧化钠溶液与氯化铜溶液反应生成氢氧化铜蓝色沉淀,化学方程式为2NaOH+CuCl2═Cu(OH)2↓+2NaCl,属于复分解反应;(3)由于氢氧化钠不与铁反应,所以能用铁器盛放氢氧化钠固体,(4)中和反应是指酸与碱反应生成盐和水的反应,所以其中的中和反应有NaOH+HCl═NaCl+H2O 和 Ca(OH)2+2HCl═CaCl2+2H2O(5)碱的性质为:碱溶液能跟酸碱指示剂、非金属氧化物(即酸性氧化物)、酸起、某些盐反应,所以A为非金属氧化物。(6)纯碱中的碳酸根离子与氢氧化钙中的钙离子结合生成碳酸钙沉淀,故纯碱可与氢氧化钙反应;
安琪同学为探究铁制品锈蚀的条件,进行如下实验:
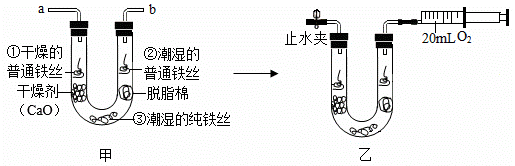
步骤1:利用图甲所示装置,将干燥的O2从导管a通入U形管(装置气密性良好,药品如图所示);待U形管内充满O2后,在导管b处连接一活塞推至底部的注射器收集20mL O2后在导管a处连接乳胶管并用止水夹夹紧,如图乙所示。
步骤2:一段时间后,观察U形管内的铁丝表面的现象如表所示。
| 观察对象 | 现象 |
| ①干燥的普通铁丝 | 没有明显变化 |
| ②潮湿的普通铁丝 | _____ |
| ③潮湿的纯铁丝 | 没有明显变化 |
(1)步骤1中,检查U形管内是否已充满O2的方法是_____。
(2)铁制品锈蚀的条件之一是需要O2,在此实验中能支持此条件的证据是_____。
(3)通过对比实验现象,此实验还可得出铁制品锈蚀的条件是_____和_____。
(4)雨后郊外的路比较泥泞,如果你的交通工具是自行车,你回来进行清洗后,采取的防锈措施是_____(填字母)
A 立即晾晒干 B 涂油漆 C 链条传动部件涂上油
现象:铁丝表面出现较多红褐色物质
(1)将带火量的木条放置在b导管口,若木条复燃,则证明U形管内已充满
(2) 观察到乙装置中注射器活塞向左移动(或注射器内O2体积减少)
(3)水分 金属的内部结构
(4)A、C
【解析】步骤2:观察U形管内的铁丝表面发生的现象。②潮湿的普通铁丝出现的现象是:铁丝表面出现较多红褐色物质;(1)步骤1中,检查U形管内是否已充满O2的方法是:在b口放带火星的木条,如果木条复燃,则装满氧气;(2)铁制品锈蚀的条件之一是需要 O2,在此实验中能支持此条件的证据是:潮湿的普通铁丝,通入氧气后,有较多红褐色锈斑,注射器中氧气减少;(3)通过对比实验现象,此实验还可得出铁制品锈蚀的条件是:水分和金属的内部结构,因为①和②可以得出需要水分,②和③(即“潮湿的纯铁丝”和“潮湿的普通铁丝”)可以得出的是铁中“有无碳和其他杂质”,也就是金属的内部结构,也会影响铁是否生锈;(4)清洗后的自行车先使水分蒸发干燥后,再涂上油能防止生锈,因为生锈的条件是与水和氧气接触,涂上油防止与氧气和水接触,故选A、C。
本卷还有35题,登录并加入会员即可免费使用哦~

该作品由: 用户六安路分享上传
可圈可点是一个信息分享及获取的平台。不确保部分用户上传资料的来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系 可圈可点 ,我们核实后将及时进行处理。