用铁片与稀硫酸反应制取氢气时,下列措施不能使氢气生成速率加大的是( )
A.对该反应体系加热 B.不用稀硫酸,改用98%的浓硫酸
C.向H2SO4中通入HCl气体 D.不用铁片,改用铁粉
B
下列事实能用勒夏特列原理解释的是( )
A.煅烧粉碎的黄铁矿矿石有利于SO2的生成
B.合成氨工业中使用铁触媒做催化剂
C.用饱和食盐水除去氯气中氯化氢杂质
D.容器中有2NO2(g)![]() N2O4(g),增大压强颜色变深
N2O4(g),增大压强颜色变深
C
NaHSO3溶液在不同温度下均可被过量KIO3氧化,当NaHSO3完全消耗即有I2析出,依据I2析出所需时间可以求得NaHSO3的反应速率。将浓度均为0.020 mol·L-1NaHSO3溶液(含少量淀粉)10.0 mL、KIO3(过量)酸性溶液40.0 mL混合,记录10~55 ℃间溶液变蓝时间,55 ℃时未观察到溶液变蓝,实验结果如图。据图分析,下列判断正确的是( )
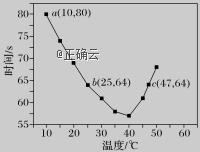
A.40 ℃之前,温度升高反应速率减慢,变蓝时间变长
B.40 ℃之后溶液变蓝的时间随温度的升高变短
C.图中b、c两点对应的NaHSO3的反应速率相等
D.图中a点对应的NaHSO3的反应速率为5.0×10-5mol·L-1·s-1
D
.在密闭容器中进行反应:X(g)+3Y(g)![]() 2Z(g),有关下列图像的说法错误的是( )
2Z(g),有关下列图像的说法错误的是( )
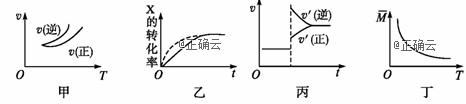
A.依据图甲可判断正反应为放热反应
B.在图乙中,虚线可表示使用了催化剂
C.若正反应的ΔH<0,图丙可表示升高温度使平衡向逆反应方向移动
D.由图丁中气体平均相对分子质量随温度的变化情况,可推知正反应的ΔH>0
D
可逆反应 2NO2(g)![]() N2O4 (g)在体积不变的密闭容器中反应,达到平衡状态的标志是( )
N2O4 (g)在体积不变的密闭容器中反应,达到平衡状态的标志是( )
①单位时间内生成 n mol N2O4 的同时生成 2n mol NO2
②单位时间内消耗 n mol N2O4的同时生成 2n mol NO2
③用NO2、N2O4的物质的量浓度变化表示的反应速率的比为2:1 的状态
④混合气体的颜色不再改变的状态
⑤混合气体的平均相对分子质量不再改变的状态
A. ①④⑤ B. ②⑤ C. ①③④ D. ①②③④⑤
A
本卷还有13题,登录并加入会员即可免费使用哦~

该作品由: 用户孙随新分享上传
可圈可点是一个信息分享及获取的平台。不确保部分用户上传资料的来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系 可圈可点 ,我们核实后将及时进行处理。