人们可以对物质从不同的角度进行分类。请根据示例将酒精、醋酸、水、食盐四种物质进行分类,并写出分类依据。
| 不同类的物质 | 分类依据 | |
| 示例 | 食盐 | 常温下食盐是固体,其余是液体 |
| 分类一 | ||
| 分类二 |
【答案】(凡合理答案均可)
| 不同类的物质 | 分类依据 | |
| 分类一 | 水 | 水是氧化物,其余不是氧化物 |
| 分类二 | 醋酸 | 醋酸是酸,其余不是酸 |
【解析】根据水是氧化物而其余的不是氧化物分类,根据醋酸是酸,其余的不是酸分类等。
实验室要配制50 g溶质质量分数为20%的硫酸钠溶液,现有25 g溶质质量分数为40%的硫酸钠溶液、20 g溶质质量分数为15%的硫酸钠溶液及足够多的硫酸钠固体和蒸馏水,请选用上述药品,设计两种配制方案填入下表中。
| 配制方案(只要说明配制时所需的各种药品及用量即可) | |
| 方案一 | |
| 方案二 |
方案一 10 g硫酸钠和40 g水
方案二 25 g溶质质量分数为40%的硫酸钠溶液和25 g水
【解析】开放型题只要答案合理即可,但也正是因为开放,许多同学在答题时感觉无从下手。就本题来说,配制50 g20%的硫酸钠溶液,一是利用硫酸钠和水配制,需硫酸钠的质量:50 g×20%=10 g,则需水的质量为40 g;二是向25 g 40%的硫酸钠溶液中加水,设加水质量为m,则
![]() m=25 g
m=25 g
有三种白色粉末,分别是碳酸钡、硫酸钡和碳酸钠。请设计一个实验方案,把这三种粉末区分开来。叙述实验操作、预期现象与结论。
(实验室仅提供了稀盐酸、Na2SO4溶液、蒸馏水以及常用的实验仪器)
| 实验操作 | 预期现象与结论 |
【答案】(合理即可)
| 实验操作 | 预期现象与结论 |
| 取三种白色粉末适量,分别置于三个洁净的小烧杯中,向每个小烧杯中加入足量的蒸馏水,并用玻璃棒搅拌 | 其中有两个小烧杯中的白色粉末不溶于水,另外一个小烧杯中的白色粉末完全溶解于水,则白色粉末完全溶解的小烧杯中的原物质为Na2CO3 |
| 向粉末不溶于水的两个小烧杯中分别加入足量的稀盐酸,并用玻璃棒搅拌 | 其中一个小烧杯中的白色粉末完全溶解,并且溶液中有气泡冒出,则该小烧杯中的原白色粉末为BaCO3;另外一个小烧杯中的白色粉末仍然不溶,则该小烧杯中的原白色粉末为BaSO4 |
【解析】此题是一道物质的鉴别题,根据所提供的试剂,可采用以下方法:
方法一:先根据它们在水中的溶解性不同(BaCO3、BaSO4不溶,Na2CO3可溶)用蒸馏水鉴别出Na2CO3;然后根据BaCO3和BaSO4在稀盐酸中的溶解情况不同(BaCO3能溶于稀盐酸产生气泡、BaSO4不溶于稀盐酸)用稀盐酸将二者区分出来。
方法二:先用稀盐酸鉴别出BaSO4(BaCO3和Na2CO3能溶于稀盐酸产生气泡,而BaSO4与稀盐酸不反应);再用蒸馏水鉴别BaCO3和Na2CO3(BaCO3不溶于水,而Na2CO3能溶于水)。
方法三:先用稀盐酸鉴别出BaSO4(BaCO3和Na2CO3能溶于稀盐酸产生气泡,而BaSO4与稀盐酸不反应);再向上述产生气泡的两种溶液中分别滴加Na2SO4溶液,出现沉淀的原物质是BaCO3,不产生沉淀的原物质是Na2CO3。
小明暑假期间到农田施肥时,发现撒落在地上的碳酸氢铵在阳光的照射下很快消失了,同时有浓烈的刺激性气味。他很好奇,返校后和同学们进行探究,请你一同参与:
【提出问题】温度较高时,碳酸氢铵能分解吗?产物是什么?
【猜想假设】碳酸氢铵受热易分解,产物可能为水、二氧化碳、氨气。
【实验设计】小明设计了如图所示的装置进行实验(夹持装置省略)。
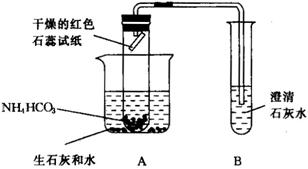
(1)根据现象: ,证明实验后生成了水和氨气。
(2)装置B中澄清石灰水 ,证明产物中有二氧化碳生成。
(3)小红同学认为若将装置B中澄清石灰水改为NaOH溶液,再通过实验验证B中产物,也可以证明碳酸氢铵分解后有二氧化碳生成。请你帮她设计并完成验证B中产物的实验:
| 实验步骤 | 实验现象 | 反应的化学方程式 |
【实验结论】碳酸氢铵受热易分解,其反应的化学方程式为 。
【实验评价】在上述同学们的探究活动中,你最欣赏的是________。
【实验反思】根据以上实验,你认为碳酸氢铵化肥在存放时应注意的问题是 。
(1)干燥的红色石蕊试纸变蓝 (2)变浑浊
(3)
| 实验步骤 | 实验现象 | 反应的化学方程式 |
| 取装置B中溶液少许,滴加稀盐酸(或滴加氯化钙溶液或氢氧化钡溶液) | 产生气泡(或产生白色沉淀) | Na2CO3+2HCl=2NaCl+CO2↑ [或Na2CO3+CaCl2=CaCO3↓+2NaCl 或Na2CO3+Ba(OH)2=BaCO3↓+2NaOH] |
(其他合理答案也可)
【实验结论】NH4HCO3![]() NH3↑+H2O+CO2↑
NH3↑+H2O+CO2↑
【实验评价】小明同学用生石灰和水反应放出的热量做热源(或小红同学验证二氧化碳的方法)(其他合理答案也可)
【实验反思】应避光、避热、密封
【解析】
(1)鉴别NH3可用湿润的红色石蕊试纸,若变蓝证明是氨气;干燥试纸能变蓝,说明有水生成,因为NH3遇水生成NH3·H2O,NH3·H2O显碱性;
(2)澄清石灰水变浑浊,一定产生CO2气体;
(3)CO2与NaOH反应生成Na2CO3(溶于水)和H2O,只要证明有Na2CO3存在即可证明产生了CO2。
若从硫酸、硫酸钠、碳酸钠、氢氧化钡、氯化钠、硝酸钠、硝酸铜、硝酸八种溶液取出其中的两种,进行混合及有关实验,实验操作和观察到的现象如下所示。
| 步骤 | 实验操作 | 实验现象 |
| ① | 将取出的两种溶液混合 | 混合溶液无色、澄清,无其它明显现象 |
| ② | 用pH试纸测定混合溶液的pH | 测定结果:pH=0 |
| ③ | 向混合溶液中滴入足量硝酸钡溶液 | 有白色沉淀出现 |
| ④ | 向上述混合物过滤所得的滤液中滴加硝酸银溶液 | 无明显现象 |
试根据各步实验现象回答下列问题:
(1)所取出的两种溶液的可能组合(写溶质的化学式,有几组要写几组) _ 。
(2)写出步骤③可能发生反应的化学方程式 。
(1)可能组合:①H2SO4和Na2SO4 ②H2SO4和NaNO3 ③H2SO4和HNO3 ④HNO3和Na2SO4
(2) Ba(NO3) 2+ H2SO4 = BaSO4↓+2HNO3
Ba(N03)2+ Na2SO4 =BaSO4↓+2NaNO3
本卷还有5题,登录并加入会员即可免费使用哦~

该作品由: 用户小小分享上传
可圈可点是一个信息分享及获取的平台。不确保部分用户上传资料的来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系 可圈可点 ,我们核实后将及时进行处理。