某可燃化合物×完全燃烧的化学方程式为X+O2→CO2+H2O(未配平)则X不可能是( )
A. CO ![]() B. CH4
B. CH4 ![]() C. 甲醇(CH3OH)
C. 甲醇(CH3OH) ![]() D. 乙醇(CH3CH2OH)
D. 乙醇(CH3CH2OH)
【答案】A
【解析】【解答】根据质量守恒定律可知,反应物和生成物中的元素种类相同,如果反应物X是一氧化碳,则反应物中的元素有碳元素和氧元素,生成物中不可能含有氢元素,所以X不可能是一氧化碳.
故选A.
【分析】在化学反应中遵循质量守恒定律,即反应前后元素的种类不变,原子的种类、个数不变.在化学反应中遵循质量守恒定律,参加反应的物质的质量总和等于反应后生成的物质的质量总和.
在一密闭容器内有4种物质,通过电火花引燃后发生充分反应,测得反应前后各物质的质量如下表:
| 甲 | 乙 | 丙 | 丁 | |
| 反应前的质量/g | 4 | 10 | 1 | 25 |
| 反应后的质量/g | 未测定 | 21 | 10 | 9 |
已知丁的相对分子质量为甲的2倍,则该反应的化学方程式中甲与丁的化学计量数的比为( )
A. 1:1 ![]() B. 1:2
B. 1:2 ![]() C. 1:3
C. 1:3 ![]() D. 2:1
D. 2:1
【答案】B
【解析】【解答】解:根据质量守恒定律,由表中乙、丙质量增加,可确定乙、丙为生成物,共增加了(21﹣10)g+(10﹣1)g=20g,
丁减少了(25﹣9)g=16g,减少的质量还差(20﹣16)g=4g,由此可知4g甲完全反应无剩余.
即甲、丁反应时的质量比为4g:16g=1:4.
设该反应的化学方程式中甲与丁的化学计量数的比为m:n,又丁的相对分子质量为甲的2倍,则
m:2n=1:4,解得m:n=1:2.
故选B.
【分析】根据质量守恒定律,由物质质量的增减可确定反应物和生成物;由增减量的多少可确定反应物和生成物的质量关系,再结合甲、丁的相对分子质量关系得出本题答案.
已知 2NaClO3+H2SO4+SO2=2X+2NaHSO4 由此可知X物质的化学式为( )
A. ClO2 B. NaCl C. NaClO D. Cl2O
【答案】A
【解析】由质量守恒定律:反应前后,原子种类、数目均不变,由反应的化学方程式2NaClO3+H2SO4+SO2═2X+2NaHSO4 , 反应前钠、氯、氧、氢、硫原子个数分别为2、2、6、10、2、2,反应后的生成物中钠、氯、氧、氢、硫原子个数分别为2、0、8、2、2,根据反应前后原子种类、数目不变,则,2X分子中含有2个氯原子和4个氧原子,则每个X分子由1个氯原子和2个氧原子构成,则物质X的化学式为ClO2。
故答案为:A。
【分析】本题有两种结题思路,一种是质量守恒定律,反应前后原子数目是不变的,通过等式左右两边的原子数目,判断答案为A,另一种是通过化学方程式的配平来解答
在密闭容器内进行的某反应中,测得反应前(t0)、反应中(t1)、反应后(t2)不同时刻甲、乙、丙、丁四种物质的质量分数分别如下图所示,则下列说法不正确的是( )
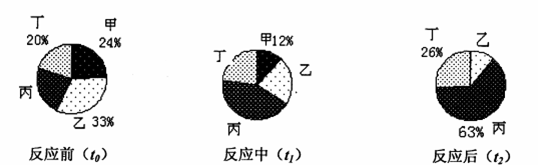
A. t1时刻,乙、丁、丙所占的质量分数分别为22%、23%和43% ![]() B. 若反应前甲、乙、丙、丁四种物质的总质量为100克,则再增加12克甲,甲与乙则恰好
B. 若反应前甲、乙、丙、丁四种物质的总质量为100克,则再增加12克甲,甲与乙则恰好
C. 该反应既不可能是化合反应,也不可能是分解反应 ![]() D. 若甲和丁分别是镁和碳,则该反应中甲和丁的化学计量数之比为1:2
D. 若甲和丁分别是镁和碳,则该反应中甲和丁的化学计量数之比为1:2
【答案】D
【解析】【解答】A、反应前丙的质量分数是1-20%-24%-33%=23%,反应后乙的质量分数为1-26%-63%=11%,参加反应的甲、乙、丙、丁的质量比为24%:(33%-11%):(63%-23%):(26%-20%)=12:11:20:3,t1时刻,甲反应掉12%,则乙反应掉11%,丁、丙分别生成3%、20%,因此乙、丁、丙所占的质量分数分别为22%、23%和43%,A不符合题意;
B、若反应前甲、乙、丙、丁四种物质的总质量为100克,则反应前甲的质量为24g,乙33g,再增加12克甲,则反应前甲乙质量比为(24g+12g):33g=12:11,所以甲与乙则恰好完全反应,B不符合题意;
C、该反应中甲乙是反应物,丙丁是生成物,所以该反应既不可能是化合反应,也不可能是分解反应,C不符合题意;
D、若甲和丁分别是镁和碳,则该反应中甲和丁的化学计量数之比为 ![]() =2:1,D符合题意。
=2:1,D符合题意。
【分析】根据质量守恒定律分析,即化学变化中参加反应的各物质质量总和等于反应后生成的各物质的质量总和;根据化学计量数即为化学方程式中化学式前的配平系数分析。
关于化学方程式2H2+O2![]() 2H2O的读法正确的是( )
2H2O的读法正确的是( )
A. 每2个氢分子和1个氧分子在点燃条件下发生反应,生成2个水分子
B. 氢和氧在点燃条件下化合生成水
C. 氢元素和氧元素在点燃条件下反应生成水
D. 每4g氢气跟32g氧气在点燃的条件下反应生成36g水
【答案】A
【解析】【解答】解:
A、由2H2+O2![]() 2H2O可知,每2个氢分子和1个氧分子在点燃条件下发生反应,生成2个水分子.故选项正确;
2H2O可知,每2个氢分子和1个氧分子在点燃条件下发生反应,生成2个水分子.故选项正确;
B、应该是氢气和氧气在点燃条件下化合生成水.故选项错误;
C、应该是氢气和氧气在点燃条件下化合生成水.故选项错误;
D、应该是每4份质量的氢气跟32份质量的氧气在点燃的条件下完全反应生成36份质量的水.故选项错误.
故选A.
【分析】化学方程式的含义有:反应物和生成物的种类;反应的条件;反应物和生成物的微观粒子个数比;反应物和生成物的质量比等.
本卷还有26题,登录并加入会员即可免费使用哦~

该作品由: 用户940603分享上传
可圈可点是一个信息分享及获取的平台。不确保部分用户上传资料的来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系 可圈可点 ,我们核实后将及时进行处理。