有X、Y、Z三中金属,将三种金属分别浸入稀硫酸在,X溶解并放出氢气,X、Z不溶解;将Y、Z分别浸入硝酸银溶液中,在Y的表面有银析出,而Z不反应.则三种金属的活动性由强到弱排列顺序是( )
A.X>Y>Z B.X>Z>Y C.Y>X>Z D.Z>Y>Z
【考点】金属活动性顺序及其应用.
【专题】金属与金属材料.
【分析】在金属活动性顺序中,只有氢前的金属可以和稀酸反应(除稀硝酸)生成氢气,只有前面的金属可以把排在它后面的金属从它的盐溶液中置换出来,根据这一规律可以判断金属的活动性强弱.
【解答】解:由于这三种金属只有金属X可以和稀硫酸反应生成氢气,说明只有X在氢前,即X的金属活动性最强;将Y、Z分别浸入硝酸银溶液中,在Y的表面有银析出,而Z不反应.说明了Y的金属的活动性大于Z,由以上分析可知,三种金属的活动性由强到弱排列顺序是:X>Y>Z.
故选:A.
【点评】本题难度不是很大,主要考查了根据反应的发生来判断金属的活动性强弱,从而加深学生对金属活动性顺序的理解和应用.
在托盘天平两边各放一只烧杯,调节至平衡,再向两只烧杯中各注入相同质量、相同质最分数的稀硫酸,然后按如图所示分别投入相同质量的锌粒和镁带,当镁条和锌粒完全溶解后,天平指针( )
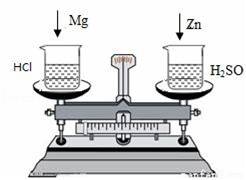

A.偏左 B.偏右 C.居中 D.无法判断
【考点】金属的化学性质.
【专题】金属与金属材料.
【分析】反应物放在一起不反应的状态时,天平是平衡的,指针的偏转主要是看生成氢气的多少,因此解题时判断氢气多少则成为解题的关键所在.
【解答】解:锌粒和镁条全部溶解,说明酸足量,设金属的质量为65,镁生成的氢气质量为y
Zn+2HCl═ZnCl2+H2↑
65 2
生成的氢气是2
Mg+H2SO4═MgSO4+H2↑
24 2
65 y
![]()
![]()
y=5.4
镁生成的氢气多,指针偏右.
故选B.
【点评】本题考查了金属与酸反应生成氢气质量的关系,完成此题,可以依据反应的化学方程式,从酸的质量和金属的质量的角度进行.
两个烧杯中装有等质量的金属锌和镁,然后分别逐渐加入同浓度的稀硫酸,产生氢气的质量与加入硫酸的质量关系如图所示,下列说法正确的是( )


A.a点时,两个烧杯中的酸都恰好完全反应
B.b点时,两个烧杯中产生氢气的质量相同
C.c点时,两个烧杯中都有金属剩余
D.该图反映出镁比锌的金属活动性强
【考点】金属的化学性质.
【专题】金属与金属材料.
【分析】根据镁、锌金属活动性均比氢强,均能与稀硫酸反应,等质量的金属锌和镁,分别逐渐加入同浓度的稀硫酸,由生氢气的质量与加入硫酸的质量关系图,最终镁产生的氢气质量多,进行分析判断.
【解答】解:A、a点时,镁与稀硫酸恰好完全反应,锌早已完全反应,故A错误;
B、b点时,镁产生的氢气多,锌产生的氢气质量少,故B错误;
C、c点时,锌与镁均还没有完全反应,两个烧杯中都有金属剩余,故C正确;
D、由产生氢气的质量与加入硫酸的质量关系图,镁产生的氢气质量多,但无法得出镁与锌的金属活动性的关系,故D错误.
故选:C.
【点评】本题难度不大,理解产生氢气的质量与加入硫酸的质量关系图的含义,掌握金属的化学性质是正确解答本题的关键.
金属材料在人类活动中已得到越来越广泛的应用.下列性质属于金属共性的是( )
A.硬度很大、熔点很高 B.是银白色的固体
C.易与酸反应产生氢气 D.能够导电、能够导热
【考点】金属的物理性质及用途.
【专题】金属与金属材料.
【分析】可以根据金属的性质方面进行分析、判断,从而得出正确的结论.例如,一些金属较软,一些金属熔点较低.都有良好的导电性、导热性.颜色不都是银白色的.一些金属不能和酸反应.
【解答】解:
A、一些金属的硬度很小,熔点较低,如钠等,故A错误;
B、一些金属的颜色不是银白色的,例如铜是红色的,故B错误;
C、铜不能和稀盐酸反应,故C错误;
D、金属都有良好的导电性、传热性,故D正确.
故选:D.
【点评】解答本题的关键是要充分了解金属的性质,只有这样才能对问题做出正确的判断.
用品,要利用金属导热性的是( )
A.
 B.
B.
 C.
C.
 D.
D.

【考点】金属的物理性质及用途.
【专题】金属与金属材料.
【分析】物质的性质决定了物质的用途,所以可以根据铁的用途,分析利用了金属的什么性质.
【解答】解:A、利用金属的金属的光泽,错误;
B、利用金属的导电性,错误;
C、利用金属的延展性,错误;
D、利用金属的导热性,正确;
故选D.
【点评】本题主要考查了金属、合金的性质和用途,难度不大,需要在平时多加记忆即可解答.
本卷还有17题,登录并加入会员即可免费使用哦~

该作品由: 用户王胜分享上传
可圈可点是一个信息分享及获取的平台。不确保部分用户上传资料的来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系 可圈可点 ,我们核实后将及时进行处理。