某化学兴趣小组的同学向一定量的NaHCO3溶液中加入一定量的稀H2SO4。待反![]() 应完全后(假设反应产生的气体全部逸出),对反应后溶液中溶质的成分进行如下探究:
应完全后(假设反应产生的气体全部逸出),对反应后溶液中溶质的成分进行如下探究:
【实验用品】pH试纸、Zn片、氧化铜粉末、稀H2SO4、NaOH溶液、BaCl2溶液。
【假设猜想】猜想一:Na2SO4 猜想二:Na2SO4、NaHCO3 猜想三:Na2SO4、H2SO4
【实验探究】同学们取反应后的溶液用不同方案进行如下实验,请根据现象或结论填空。
| 实验方案 | A | B | C | D |
| 实验操作 |
|
|
|
|
| 实验现象 | 无气泡产生 | 试纸变色,对照 比色卡,pH<7 | ___________ ___ | 产生白色沉淀 |
| 实验结论 | ________ | 猜想三正确 | 猜想三正确 | 猜想三正确 |
【得出结论】猜想三正确。
【评价反思】老师对同学们能用多种方案进行探究,并且得出正确的实验结论给予了肯定,同时指出探究中存在两处明显错误。分别是:①_________ ;
②___________ 。
【总结提高】依据所给实验用品,你还有什么不同类方案确认猜想三是正确的。请写出你的实验方案___________
。
【实验探究】A:猜想二不正确 C:有气泡产生,锌片不断溶解
【评价反思】①方案B中pH试纸浸入溶液中 ②方案D中硫酸钠与氯化钡反应也会生成白色沉淀,不能证明一定有H![]() 2SO4存在 【总结提高】取少量氧化铜粉末于试管中,加入足量反应后的溶液,若黑色固体溶解,溶液变蓝,则猜想三正确(合理即可)
2SO4存在 【总结提高】取少量氧化铜粉末于试管中,加入足量反应后的溶液,若黑色固体溶解,溶液变蓝,则猜想三正确(合理即可)
【解析】A方案是利用碳酸氢钠能与稀硫酸反应,通过滴加稀硫酸,如果产生气泡,说明溶液中含有碳酸氢钠,猜想二正确,如果没有气泡产生,说明溶液中没有碳酸氢钠,即猜想二不正确;B方案是利用测定溶液酸碱度,判断溶液中的溶质,测定溶液酸碱度时,不能将pH试纸直接伸入待测溶液中,否则会污染试剂,应用玻璃棒蘸取或用胶头滴管吸取少量待测液滴于pH试纸上,如果pH<7,说明溶液中含有硫酸,猜想三正确;方案C是利用稀硫酸能与锌反应,通过反应后溶液与锌片接触是否产生气泡,判断是否有硫酸;方案D是想利用硫酸能与氯化钡反应生成硫酸钡白色沉淀,说明有硫酸,但这一方案是错误的,原因是硫酸钠也能与氯化钡反应生成硫酸钡白色沉淀,此外可利用硫酸能与氧化铜反应生成硫酸铜和水,用氧化铜检验溶液中是否有硫酸。
某化学学习小组的同学对一瓶久置的氢氧化钠的化学成分产生了兴趣,他们根据自己已学的知识进行如下探究,请你共同参与并填空:
【猜想假设】
猜想一:只有氢氧化钠;猜想二:是氢氧化钠和碳酸钠的混合物;
猜想三:____________________。
【查阅资料】
(1)BaCl2溶液显中性; (2)Na2CO3溶液与BaCl2溶液能反应产生白色沉淀。
【实验探究】
| 实验步骤 | 实验现象 | 实验结论 |
| (1)用小试管取少量固体样品加水完全溶解,再滴加过量BaCl2溶液 | 产生白色 沉淀 | 猜想______不正确 |
| (2)取(1)中的少量上层清液于试管中,滴加酚酞试液 | ________ | 猜想二正确,猜想三不正确 |
【实验结论】
该氢氧化钠样品已部分变质,其化学成分是NaOH与Na2CO3的混合物,引起NaOH变质的化学方程式为___________________________
_________。
【反思交流】
(1)实验室应________保存氢氧化钠。
(2)某同学认为用CaCl2溶液代替BaCl2溶液也可以得到同样的结论,另一位同学认为不可以,理由是:CaCl2溶液和NaOH溶液相混合也会出现____________,因为Ca(OH)2是________________。
【猜想假设】只有碳酸钠 【实验探究】(1)一 (2)溶液变红
【实验结论】2NaOH+CO2=== Na2CO3+H![]() 2O 【反思交流】(1)密封 (2)白色沉淀 微溶于水的物质
2O 【反思交流】(1)密封 (2)白色沉淀 微溶于水的物质
【解析】【猜想假设】氢氧化钠溶液与空气中的二氧化碳反应生成碳酸钠和水,如果氢氧化钠全部变质,则只有碳酸钠;【实验探究】(1)氯化钡溶液与碳酸钠反应生成碳酸钡白色沉淀和氯化钠,根据实验现象,可知固体样品中含有碳酸钠,猜想一不正确。(2)向(1)中的少量上层清液中滴加酚酞试液,根据实验结论可得氢氧化钠是部分变质,加入过量BaCl2溶液后,除去了CO![]() ,上层清液中含有氢氧化钠、氯化钡,故
,上层清液中含有氢氧化钠、氯化钡,故![]() 滴加酚酞试液后溶液变红色。【实验结论】氢氧化钠溶液与二氧化碳反应生成碳酸钠和水。【反思交流】(1)氢氧化钠露置于空气中容易变质,需密封保存。(2)氯化钙溶液中的钙离子与氢氧化钠溶液中的氢氧根离子结合,产生微溶于水的氢氧化钙,也会出现白色沉淀。
滴加酚酞试液后溶液变红色。【实验结论】氢氧化钠溶液与二氧化碳反应生成碳酸钠和水。【反思交流】(1)氢氧化钠露置于空气中容易变质,需密封保存。(2)氯化钙溶液中的钙离子与氢氧化钠溶液中的氢氧根离子结合,产生微溶于水的氢氧化钙,也会出现白色沉淀。
为确定木炭还原氧化铜后的固体成分,请你与兴趣小组的同学完成以下探究:
【对固体猜想】
猜想Ⅰ:全部是金属铜; 猜想Ⅱ:除铜外,还含有氧化铜;
猜想Ⅲ:除铜外,还含有木炭; 猜想Ⅳ:除铜外,还含有氧化铜、________。
【进行实验】实验流程见下图:
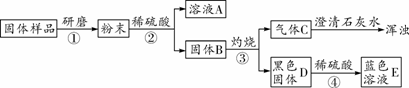
第3题图
【问题与讨论】
(1)步骤②包括溶解、________两步操作,它们共同用到的玻璃仪器是烧杯、________。
(2)C的化学式为________,D的化学式为________,由此推出固体B中含有________(写化学式),步骤④发生反应的化学方程式为______________________。
(3)结合(2)的结论推断:如果溶液A显蓝色,则溶液A的溶质的化学式为________,说明样品中含有________,则证明猜想________成立;如果溶液A无色,则证明猜想________成立。
【对固体猜想】猜想Ⅳ:木炭 【问题与讨论】(1)过滤 玻璃棒 (2)CO2 CuO C和Cu CuO+H2SO4=== CuSO4+H2O (3)CuSO4 氧化铜(或CuO) Ⅳ Ⅲ
【解析】此题是一道探究性实验题,试题以木炭还原氧化铜为题材进行设计,通过分析探究反应后剩余固体的成分,考查考生分析解决实际问题的能力。木炭还原氧化铜实验后剩余固体的成分中一定有铜,还可能有剩余的木炭或氧化铜,根据试题的几种猜想很容易回答猜想Ⅳ:除铜外,还含有氧化铜、木炭。在实验流程图步骤②中稀硫酸只与氧化铜反应,不与铜、也不与木炭反应,通过过滤可将溶液A与固体B分离。对固体B灼烧生成的气体C(CO2)可使澄清的石灰水变浑浊,表明固体B中含有木炭。灼烧得到的黑色固体D可与稀硫酸反应生成蓝色溶液E(硫酸铜溶液),可知黑色固体为氧化铜,进而可知固体B中含有铜,据此可推出固体B中有C和Cu。根据实验现象若溶液A呈蓝色,表明样品中含有氧化铜,氧化铜与稀硫酸反应生成蓝色的硫酸铜溶液,剩余固体为铜、氧化铜和木炭,证明猜想Ⅳ成立;若溶液A无色,表明样品中不含氧化铜,剩余固体成分为铜和木炭,证明猜想Ⅲ成立。
松花皮蛋是我们喜爱的食品。某小组同学查阅资料得知,制作皮蛋料泥的原料主要是:生石灰、纯碱、草木灰(含K2CO3)等。同学们对料泥进行了如下探究:
【猜想】猜想Ⅰ:料泥的主要成分是Ca(OH)2、NaOH、KOH、CaCO3、灰分;
猜想Ⅱ:料泥的主要成分是NaOH、KOH、Na2CO3、CaCO3、灰分。
【实验与现象】实验过程与现象如下图:
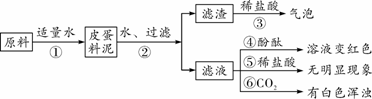
第6题图
【问题与讨论】
(1)步骤②中所需要的玻璃仪器有:烧杯、玻璃棒、________,玻璃棒在步骤②中的一种作用________________。
(2)步骤③的现象说明滤渣中含有:____________(写化学式)。
(3)请写出步骤①发生的任意两个反应的化学方程式:__________________________、____________________________。
(4)由上述实验现象推断,猜想______是正确的,其理由是________________________。
(1)漏斗 搅拌,加速溶解(或引流,防止溶液外溅)
(2)CaCO3
(3)CaO+H2O===Ca(OH)2 Na2CO3+Ca(OH)2===CaCO3↓+2NaOH[或K2CO3+Ca(OH)2===CaCO3↓+2KOH] (4)Ⅰ步骤⑤无明显现象,说明料泥中无Na2CO3;步骤⑥有白色浑浊,说明料泥中有Ca(OH)2
钠盐种类较多,在实验室里,钠盐通常都摆放在同一药品柜中。小华所在的化学兴趣小组在整理药品柜时,发现某试剂瓶外壁两边贴上了新旧两个标签,分别是“Na2SO4溶液”、“Na2CO3溶液”,小华认为其原因是:Na2CO3溶液的试剂瓶混入了Na2SO4溶液,并加贴了新标签。该兴趣小组对溶液的成分进行了探究。请你完成以下探究过程。
【提出问题】①______________________________________。
【提出猜想】猜想Ⅰ:溶质仅为Na2SO4;猜想Ⅱ:溶质仅为Na2CO3;猜想Ⅲ:溶质为Na2SO4和Na2CO3。
【实验探究】
| 实验操作 | 实验现象 | 实验结论 |
| 1. 取少量样品于一支洁净试管中,加入足量稀硫酸 | ②____________ | 猜想Ⅰ不成立 |
| 2. ③________________ ______,向其中加入过量的BaCl2溶液,过滤,向所得沉淀中加入足量稀硝酸 | 先产生白色沉淀;加入硝酸溶液后,有气泡产生,沉淀部分溶解 | 猜想④______成立 |
【问题讨论】试写出加入BaCl2溶液后,生成不溶于硝酸的白色沉淀的化学方程式⑤________________________。
【提出问题】①该试剂瓶内溶质的化学成分是什么? 【实验探究】②有气泡产生 ③取少量样品于另一支洁净的试管中 ④Ⅲ
【问题讨论】⑤Na2SO4+BaCl2=== BaSO4↓+2NaCl
【解析】【提出问题】根据猜想和信息可知,提出的问题是该试剂瓶内溶质的化学成分是什么?【实验探究】猜想Ⅰ不成立,说明溶液中的溶质含有碳酸钠,碳酸钠与稀硫酸反应会生成二氧化碳,可观察到有气泡产生;根据实验1的操作可知,实验2的操作是:取少量样品于另一支洁净的试管中;观察到的现象:先产生白色沉淀,加入稀硝酸后,有气泡产生,沉淀部分溶解,说明生成![]() 的沉淀既有碳酸钡也有硫酸钡,则原溶液中的溶质有硫酸钠和碳酸钠,则猜想Ⅲ成立。【问题讨论】生成的不溶于硝酸的白色沉淀是硫酸钡,反应的化学方程式为Na2SO4 + BaCl2 === BaSO4↓ + 2NaCl。
的沉淀既有碳酸钡也有硫酸钡,则原溶液中的溶质有硫酸钠和碳酸钠,则猜想Ⅲ成立。【问题讨论】生成的不溶于硝酸的白色沉淀是硫酸钡,反应的化学方程式为Na2SO4 + BaCl2 === BaSO4↓ + 2NaCl。
本卷还有10题,登录并加入会员即可免费使用哦~

该作品由: 用户许小兰分享上传
可圈可点是一个信息分享及获取的平台。不确保部分用户上传资料的来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系 可圈可点 ,我们核实后将及时进行处理。