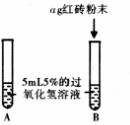
已知二氧化锰能作过氧化氢分解的催化剂,某兴趣小组想探究其他物质是否也可以作过氧化氢分解的催化剂。请参与他们的探究过程。
【提出问题】
红砖粉末能否作为过氧化氢分解的催化剂,如果能,效果如何?
【进行实验】
| 实验步骤 | 实验现象 | 实验结论及解释 |
| Ⅰ | A中无明显现象 B.中产生大量能使带火星木条复燃的气体
| ①产生的气体是________ ②红砖粉末能改变过氧化氢分解速率 |
| Ⅱ | ①又产生大量能使带火星木条复燃的气体 ②滤渣质量等于ag | 红砖粉末的________和________在反应前后均没有发生变化,能作过氧化氢分解的催化剂 |
| Ⅲ | 两试管中均产生气泡,不同之处是加入二氧化锰的试管中产生气泡的速率比加入红砖粉末的________(填“快”或“慢”) | 红砖粉末的催化效果没有二氧化锰粉末好 |
【得出结论】
故红砖粉末能作过氧化氢分解的催化剂。写出红砖粉末催化过氧化氢分解反应的文字表达式________。
【拓展延伸】
下列有关催化剂的说法正确的是________(填字母)。
A.催化剂只能加快反应速率
B.催化剂不能决定反应能否发生
C.使用催化剂能增加产物质量
【进行实验】![]() 氧气;Ⅱ
氧气;Ⅱ![]() 质量;化学性质;Ⅲ
质量;化学性质;Ⅲ![]() 快;
快;
【得出结论】过氧化氢![]() 水+氧气
水+氧气
【拓展延伸】B
【解析】【分析】
【进行实验】I.根据氧气的检验方法和现象分析;
II.根据实验结论及催化剂的定义分析解答;
III.根据实验结论分析实验现象;
【得出结论】根据过氧化氢在红砖粉末催化下分解为水和氧气书写化学反应文字表达式;
【拓展延伸】根据催化剂的特点是“一变二不变”分析解答。
【解答】
【进行实验】I.氧气具有助燃性,能使带火星的木条复燃,由该实验现象可知,产生的气体是氧气;
II.实验前后红砖粉末的质量和化学性质均没有变,但却加快了过氧化氢的分解速率,因此,红砖粉末对过氧化氢的分解具有催化作用;
III.由于红砖粉末的催化效果没有二氧化锰粉末好,所以,在其它条件相同的情况下,加入二氧化锰的试管中产生气泡的速率比加入红砖粉末的快;
【得出结论】过氧化氢在红砖粉末的催化下分解为水和氧气,反应的文字表达式为:过氧化氢![]() 水+氧气;
水+氧气;
【拓展延伸】A.有的催化剂能加快反应速率,有的催化剂能减慢化学反应速率,A错误;
B.催化剂只能改变反应速率,不能决定反应能否发生,B正确;
C.使用催化剂对反应生成物的质量无影响,C错误。
故选:B。
故答案为:
【进行实验】I.氧气;Ⅱ![]() 质量;化学性质;Ⅲ
质量;化学性质;Ⅲ![]() 快;
快;
【得出结论】过氧化氢![]() 水+氧气
水+氧气
【拓展延伸】B。
硼(B)及其化合物在工业上有许多用途.以铁硼矿(主要成分为Mg2B2O5﹒H2O和Fe3O4,还有少量Fe2O3、FeO、CaO、Al2O3和难溶性SiO2等)为原料制备硼酸(H3BO3)的工艺流程如图所示:
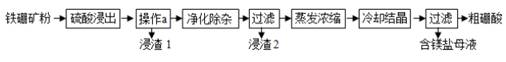
已知:①Mg2B2O5﹒H2O+2H2SO4=2MgSO4+2H3BO3
②CaSO4微溶于水
③H2O2溶液可将Fe2+氧化为Fe3+
④Fe3+、Fe2+、Fe2+以氢氧化物形式开始沉淀和完全沉淀时的pH如表:
| 开始沉淀 | 完全沉淀 | |
| Fe3+ | 1.14 | 3.0 |
| Fe2+ | 5.85 | 8.35 |
| Fe2+ | 3.0 | 4.7 |
请回答下列问题:
(1)利用______(填物质名称)的磁性,可将该物质直接从“铁硼矿粉”中分离.
(2)酸浸时,矿粉中的金属氧化物会和酸反应,试写出Fe2O3酸浸时的化学反应方程式.______
(3)为了提高浸出速率(即加快反应速率),除适当增加硫酸浓度外,还可采取的措施有______(写出一条).
(4)操作a为______,“浸渣”中含有CaSO4和______(填物质化学式).
(5)“净化除杂”需先加H2O2溶液,然后再调节溶液的pH约为5,目的是______.
(6)制得的粗硼酸中的主要杂质为______(填物质化学式).
四氧化三铁 ![]() 粉碎矿石或者加热等 过滤 SiO2 将亚铁离子转化为铁离子,进一步将铁离子和铝离子通过控制pH为5使之完全沉淀 Na2SO4
粉碎矿石或者加热等 过滤 SiO2 将亚铁离子转化为铁离子,进一步将铁离子和铝离子通过控制pH为5使之完全沉淀 Na2SO4
【解析】解:
(1)由于四氧化三铁有磁性所以对应的矿石叫磁铁矿,所以可以利用四氧化三铁的磁性,可将该物质直接从“铁硼矿粉”中分离.
(2)酸浸时,矿粉中的金属氧化物会和酸反应,Fe2O3酸浸时是氧化铁和硫酸反应生成硫酸铁和水,对应的化学反应方程式为:![]()
(3)为了提高浸出速率(![]() 即加快反应速率
即加快反应速率![]() ,除适当增加硫酸浓度外,由于接触面积越大反应越快,所以可以将矿石粉碎.同时温度越高,反应越快,所以也可以加热加速反应的进行.所以可采取的措施有粉碎矿石或者加热等.
,除适当增加硫酸浓度外,由于接触面积越大反应越快,所以可以将矿石粉碎.同时温度越高,反应越快,所以也可以加热加速反应的进行.所以可采取的措施有粉碎矿石或者加热等.
(4)操作a是固液分离,为过滤.“浸渣”中含有氧化钙和硫酸反应生成的CaSO4以及原物质含有的不溶于硫酸的 SiO2.
(5)“净化除杂”需先加H2O2溶液,然后再调节溶液的pH约为5,目的是将亚铁离子转化为铁离子,进一步将铁离子和铝离子通过控制pH为5使之完全沉淀.
(6)由于过程加入了硫酸进行酸浸以及调节pH用到氢氧化钠,制得的粗硼酸中的主要杂质为Na2SO4.
故答案为:
(1)四氧化三铁.
(2)![]()
(3)粉碎矿石或者加热等![]() 写出一条
写出一条![]() .
.
(4)过滤;SiO2.
(5)将亚铁离子转化为铁离子,进一步将铁离子和铝离子通过控制pH为5使之完全沉淀.
(6)Na2SO4.
根据给出的转化关系对应的过程分析每个对应的问题,或者直接分析每个问题,从给出的信息中找对应的信息.
读图,从中获得解答题目所需的信息,所以在解答题目时先看解答的问题是什么,然后带着问题去读给出的图进而去寻找解答有用的信息,这样提高了信息扑捉的有效性.解答的问题实际上与复杂的转化图相比,其实很简单很基础,或者可以说转化图提供的是情境,考查基本知识.
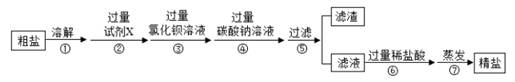
粗盐除去泥砂后含有氯化镁、硫酸钠、氯化钙等杂质,某同学对粗盐进一步提纯的实验操作过程如图所示:
(1)实验中称取5.0g粗盐,为了使粗盐充分溶解![]() 该温度下氯化钠的溶解度为36g/100g水
该温度下氯化钠的溶解度为36g/100g水![]() 量取水所用量筒的规格为______。
量取水所用量筒的规格为______。
A.10mL B.20mL C.50mL D.100mL
(2)步骤②所加试剂X的化学式为______。
(3)步骤④中加入过量碳酸钠的目的是______。
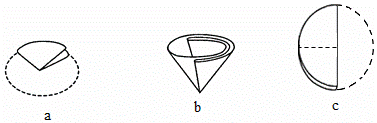
(4)步骤⑤过滤实验,制作过滤器的正确顺序为______。
过滤后所得滤渣的化学式为______。
(5)步骤⑦蒸发实验除去______(填化学式)得到精盐。
B;氢氧化钠;完全除去氯化钙和过量的氯化钡;c、a、b;![]() HCl、H2O
HCl、H2O
【解析】解:(1)设溶解5g的氯化钠至少需要水的质量x,则得:![]() ,解得:x≈13.9g 水的体积约为13.9mL,所以量取水所用量筒的规格为20mL。
,解得:x≈13.9g 水的体积约为13.9mL,所以量取水所用量筒的规格为20mL。
(2)由于氯化镁能与氢氧化钠反应生成了氢氧化镁沉淀和氯化钠,所以加入的试剂应是氢氧化钠;
(3)由于碳酸钠能与氯化钙、氯化钡反应生成了沉淀,所以步骤![]() 中加入过量碳酸钠的目的是:完全去除氯化钙和过量的氯化钡。
中加入过量碳酸钠的目的是:完全去除氯化钙和过量的氯化钡。
(4)步骤⑤过滤实验,由图示可知,制作过滤器的正确顺序为c、a、b.由于氯化镁能与氢氧化钠反应生成了氢氧化镁沉淀,氯化钡能与硫酸钠反应生成了硫酸钡沉淀,碳酸钠能与氯化钙、氯化钡反应生成了碳酸钠、碳酸钡沉淀所以,过滤后所得滤渣的化学式为:![]()
(5)由于盐酸易挥发出氯化氢气体、水受热能蒸发,所以步骤⑦蒸发实验除去HCl、H2O得到精盐。
故答为:(1)B;
(2)氢氧化钠;
(3)完全除去氯化钙和过量的氯化钡;
(4)、a、b;![]()
(5)HCl、H2O。
(1)根据氯化钠的溶解度计算、分析回答;
(2)根据氯化镁能与氢氧化钠反应生成了氢氧化镁沉淀和氯化钠分析回答;
(3)根据碳酸钠能与氯化钙、氯化钡反应分析回答;
(4)根据制作过滤器的方法和除杂质的反应分析回答;
(5)根据盐酸易挥发出氯化氢气体、水受热能蒸发分析回答。
在解此类题时,首先要知道除去的杂质的离子的性质,然后选择合适的试剂和滴加顺序进行除杂,一般加碳酸根离子要放在加钡离子之后,可以将剩余的钡离子除去,除杂的结果,最后只能剩余氯化钠,也就是氯离子和钠离子
小芳发现,氯酸钾与氧化铜混合加热,也能较快产生氧气,于是进行如下探究:
【提出猜想】除MnO2、CuO外,Fe2O3也可以作KClO3分解的催化剂.
【完成实验】按下表进行实验:测定分解温度(分解温度越低,催化效果越好).
| 实验编号 | 实验药品 | 分解温度 |
| ① | KClO3 | 580℃ |
| ② | KClO3、MnO2(质量比1:1) | 350℃ |
| ③ | KClO3、CuO(质量比l:1) | 370℃ |
| ④ | KClO3、Fe2O3(质量比1:1) | 390℃ |
【分析数据、得出结论】
(1)由实验 ______ 与实验④对比,证明猜想合理;
(2)实验所用的三种金属氧化物,催化效果最好的是 ______ .
【反思】
(3)若要证明Fe2O3是该反应的催化剂,还要验证它在化学反应前后质量和 ______ 不变.
![]() ;二氧化锰;化学性质
;二氧化锰;化学性质
【解析】解:【分析数据、得出结论】
![]() 根据催化剂能改变化学反应的速率,可选择加催化剂和不加催化剂的进行比较分解温度即可,要想证明除MnO2、CuO外,Fe2O3也可以作KClO3分解的催化剂,可选择实验①和实验④对比,证明猜想合理.
根据催化剂能改变化学反应的速率,可选择加催化剂和不加催化剂的进行比较分解温度即可,要想证明除MnO2、CuO外,Fe2O3也可以作KClO3分解的催化剂,可选择实验①和实验④对比,证明猜想合理.
![]() 分解时所需温度最低的,催化效果越好,故填MnO2;
分解时所需温度最低的,催化效果越好,故填MnO2;
【反思】
催化剂是指在化学反应里能改变其他物质的化学反应速率![]() 既能提高也能降低
既能提高也能降低![]() ,而本身的质量和化学性质在化学反应前后都没有发生改变的物质.故要证明Fe2O3是该反应的催化剂,还要验证它在化学反应前后的质量和化学性质不变
,而本身的质量和化学性质在化学反应前后都没有发生改变的物质.故要证明Fe2O3是该反应的催化剂,还要验证它在化学反应前后的质量和化学性质不变
故答案为:(1)①;(2)二氧化锰;(3)化学性质.
【分析数据、得出结论】
![]() 根据对照试验要求只有一个变量,其他条件都相同进行分析回答;
根据对照试验要求只有一个变量,其他条件都相同进行分析回答;
![]() 根据分解时所需温度最低的,催化效果越好进行分析;
根据分解时所需温度最低的,催化效果越好进行分析;
【反思】
根据催化剂的定义进行分析回答.
本题型要充分利用题目给出的信息,按照操作步骤进行实验.在进行实验对比时,要注意对照实验的可比性.本考点是中考的重要考点之一,主要出现在实验题中.影响催化效果的除了颗粒大小,还与催化剂与反应物的质量比有关.
大蒜里的化学:众所周知,大蒜是调味佐餐的佳蔬,有很多保健和医疗功能,并有极强的杀菌能力,成为《时代周刊》十大最佳营养食品之一。
【大蒜常拍碎吃是有道理的】完整的大蒜是没有气味的,这是因为在完整大蒜中所含的蒜氨酸存在于细胞质中,而大蒜细胞中还有一种蒜苷酶存在于细胞壁中,这两种物质都是无色无味的。只有在食用、切割或挤压时组织被破坏,两者结合才形成淡黄色油状、有强烈辛辣气味的大蒜素,它在酸性环境中较稳定,遇碱、受热都会分解使大蒜消炎杀菌能力下降。大蒜素就是大蒜特殊气味的来源。
【大蒜有很多妙用】去除鱼腥。鱼腥味产生的原因是由于鱼身上存在有机化学物质甲胺(化学式为CH3NH2)及其同系物(均易溶于乙醇)。因此,煮鱼时加些酒能使甲胺等溶于乙醇并在加热后挥发逸去。葱、姜、蒜中也具有挥发性的有机物,所以具有与酒相同的作用。因此,做鱼时常用葱、姜、蒜、酒去腥就是这个道理。
依据短文回答问题:
(1)大蒜组织被破坏,产生大蒜素时发生的变化属于______(填“物理变化”或“化学变化”)。
(2)甲胺溶于乙醇加热后易挥发的原因是______。甲胺溶于乙醇形成的溶液中溶剂为______。
(3)糖醋蒜有的人比较青睐,做糖醋蒜的做法科学的原因是______。
(4)甲胺中碳元素、氢元素、氮元素的质量比为______。
(5)请你根据文中信息判断,下列说法正确的是______。
A.新鲜完整的大蒜含有大量的大蒜素,杀菌能力极强
B.食用大蒜时生吃效果佳
C.大蒜能除去鱼腥,是由于大蒜中含有挥发性有机物将甲胺等溶解并在加热后挥发逸去
化学变化;温度越高,分子运动速率越快;乙醇;大蒜素在酸性条件下稳定;12:5:14;BC
【解析】解:(1)大蒜组织被破坏,产生大蒜素时有新物质生成,发生的变化属于化学变化;故填:化学变化;
(2)甲胺溶于乙醇加热后易挥发的原因是温度越高,分子运动速率越快;甲胺溶于乙醇形成的溶液中溶剂为乙醇;
故填:温度越高,分子运动速率越快;乙醇;
(3)大蒜的主要营养成份是大蒜素,糖醋蒜比较受人青睐,科学的原因是大蒜素在酸性条件下稳定,从而使大蒜素不流失;故填:大蒜素在酸性条件下稳定;
(4)根据甲胺的化学式CH3NH2;碳元素、氢元素、氮元素的质量比为:12:1×5:14=12:5:14;故填:12:5:14;
(5)根据题目信息可知:新鲜完整的大蒜不会产生大蒜素,吃大蒜时生吃效果最好,由于大蒜中含有挥发性有机物将甲胺等溶解并在加热后挥发逸去,所以大蒜能除去鱼腥;故选:BC。
(1)根据题意并结合物理变化和化学变化的判断依据分析解答;
(2)根据分子的特性及溶液的成分分析回答;
(3)根据大蒜素在酸性条件下稳定进行解答;
(4)根据化合物中各元素质量比![]() 各原子的相对原子质量
各原子的相对原子质量![]() 原子个数之比,进行分析判断;
原子个数之比,进行分析判断;
(5)根据题目信息分析解答;
本题考查的是化学与生活的知识,完成此题,可以依据已有的知识进行分析解答。
本卷还有11题,登录并加入会员即可免费使用哦~

该作品由: 用户郭万贵分享上传
可圈可点是一个信息分享及获取的平台。不确保部分用户上传资料的来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系 可圈可点 ,我们核实后将及时进行处理。